环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类投放的办法。塑料袋、废纸、旧橡胶制品等属于
| A.无机物 | B.有机物 | C.盐类 | D.非金属单质 |
在一定温度下,向2L体积固定的密闭容器中加入1molHI,2HI(g)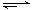 H2(g)+I2(g) △H>0,H2的物质的量随时间的变化如图示,下列说法正确的是
H2(g)+I2(g) △H>0,H2的物质的量随时间的变化如图示,下列说法正确的是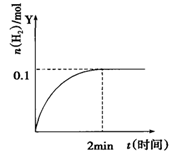
| A.该温度下,反应的平衡常数是1/8 |
| B.0~2min内的HI的平均反应速率为0.05mol•L-1•min-1 |
| C.恒压下向该体系中加入N2,平衡不移动,反应速率不变 |
| D.升高温度,平衡向正反应方向移动,只有正反应速率加快 |
能正确表示下列反应的离子方程式的是
| A.NaOH溶液中加入铝片:Al+2OH-=AlO2-+H2↑ |
B.NaHCO3溶液水解:HCO3-+H2O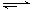 H3O+ +CO32- H3O+ +CO32- |
| C.NH4HCO3溶液与足量烧碱溶液混合:HCO3-+OH-=CO32-+H2O |
| D.硫酸溶液与氢氧化钡溶液混合:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
下列不属于有机物的是
| A.氯化钠 | B.醋酸 | C.乙炔 | D.尿素 |
12. 25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)  Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。
下列判断正确的是
| A.往平衡体系中加入少量金属铅后,c(Pb2+)增大 |
| B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
| C.升高温度,平衡体系中c(Pb2+)增大,说明该反应的△H>0 |
| D.25℃时,该反应的平衡常数K=2.2 |
一定条件下,等物质的量的N2和H2反应达平衡时,NH3的体积分数为40%,则下列叙述不正确的是
| A.N2的转化率为28.57% | B.H2的转化率为85.7% |
| C.N2的体积分数为20% | D.H2的体积分数为10% |