已知X、Y元素同周期,且电负性X>Y,下列说法错误的是 ( )
| A.X与Y形成化合物时,X显负价,Y显正价 |
| B.第一电离能Y一定小于X |
| C.最高价含氧酸的酸性:X对应的酸性弱于Y对应的酸性 |
| D.气态氢化物的稳定性:HmY小于HmX |
储氢合金表面镀铜过程发生反应Cu2++2HCHO+4OH-=Cu↓+H2↑+2H2O+2HCOO-,下列说法错误的是
| A.电镀过程中氢气在镀件表面析出 |
| B.电镀时溶液中Cu2+移向阴极,并在阴极上发生还原反应 |
| C.阳极反应式为HCHO+3OH--2e-=2H2O+HCOO- |
| D.电镀时每生成6.4g铜,镀层放出2.24L H2 |
【原创】如图用0.1mol·L-1 NaOH溶液滴定20.00 mL c1mol·L-1醋酸(含酚酞)的滴定曲线。说法正确的是
| A.A点NaOH与醋酸恰好完全反应 |
| B.醋酸的物质的量浓度为:0.10 0 mol·L-1 |
| C.V1=20ml |
| D.0~V1期间可能存在:c(CH3COO-)> c(H+)> c(Na+)> c(OH-) |
香花石被誉为“矿石熊猫”,由我国地质学家首次发现,它由前20号元素中的6种组成,其化学式为X3Y2(ZWR4)3T2,其中X、Y、Z为金属元素,Z的最外层电子数与次外层相等,X、Z位于同族,Y、Z、R、T位于同周期,R最外层电了数是次外层的3倍,T无正价,X与R原了序数之和是W的2倍。下列说法错误的是
| A.原子半径:Y>Z>R>T |
| B.气态氢化物的稳定性:W<R<T |
| C.最高价氧化物对应的水化物碱性:X>Z |
| D.XR2、WR2两化合物中R的化合价相同 |
某恒容密闭容器中的反应X(g)+Y(g) Z(g) △H<0分两步进行:
Z(g) △H<0分两步进行:
X(g)+Y(g) W(g) △H>0和W(g)
W(g) △H>0和W(g) Z(g) △H<0。下列图示有关该反应的信息不合理的是
Z(g) △H<0。下列图示有关该反应的信息不合理的是
【改编】维生素C是一种水溶性维生素(其水溶液呈酸性),又称抗坏血酸,化学式为C6H8O6,结构如下图所示。维生素C易被空气中的氧气氧化。下列关于维生素C的叙述错误的是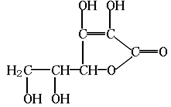
| A.维生素C能使高锰酸钾溶液褪色 |
| B.维生素C可发生取代反应 |
| C.维生素C不能与NaOH溶液发生反应 |
| D.维生素C为酯类化合物 |