北京奥运会 “祥云”火炬所用燃料为丙烷,下列有关丙烷叙述中不正确的是
| A.比甲烷的沸点高 | B.与乙烷互为同系物 |
| C.分子中的碳原子不在一条直线上 | D.可发生加成反应 |
甲基丙烯酸甲酯是世界上年产量超过100万吨的高分子单体,旧法合成的反应是:(CH3)2C===O+HCN―→(CH3)2C(OH)CN,(CH3)2C(OH)CN+CH3OH+H2SO4―→CH2===C(CH3)COOCH3+NH4HSO4。20世纪90年代新法的反应是:
CH3C CH+CO+CH3OH
CH+CO+CH3OH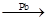 CH2===C(CH3)COOCH3,与旧法比较,新法的优点是()
CH2===C(CH3)COOCH3,与旧法比较,新法的优点是()
| A.原料无爆炸危险 |
| B.原料都是无毒物质 |
| C.没有副产物,原料利用率高 |
| D.条件比较简单 |
在有机合成中,制得的有机物较纯净并且容易分离,则在工业生产中往往有实用价值,试判断下列有机反应在工业上有生产价值的是()
A.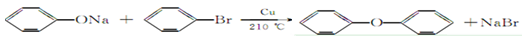 |
B.CH3—CH3+Cl2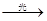 CH3—CH2Cl+HCl CH3—CH2Cl+HCl |
C.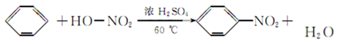 |
D.CH3COOC2H5+H2O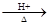 CH3COOH+C2H5OH CH3COOH+C2H5OH |
由乙醇制取环乙二酸乙二酯时,最简便的流程需要下列反应,其正确的顺序是()
①取代;②加成;③氧化;④还原;⑤消去;⑥酯化;⑦中和
| A.①②③⑤⑦ | B.⑤②①③⑥ | C.⑤②①④⑦ | D.①②⑤③⑥ |
由乙醇制乙二酸乙酯,最简单的流程途径顺序正确的是()
①取代反应 ②加成反应 ③氧化反应 ④还原反应 ⑤消去反应 ⑥酯化反应 ⑦中和反应 ⑧缩聚反应
| A.⑤②①③⑥ | B.①②③⑤⑦ | C.⑤③①②⑧ | D.①②⑤③⑥ |
由溴乙烷为主要原料制取乙二醇时,需要经过的反应为()
| A.加成—消去—取代 |
| B.消去—加成—取代 |
| C.取代—加成—消去 |
| D.取代—消去—加成 |