下列说法中错误的是:
A.SO2、SO3都是极性分子 |
||
B.在NH4+和[Cu(NH3)4]2+中都存在配位键 |
C.元素电负性越大的原子,对键合电子的吸引能力越强 |
D.离子晶体具有熔点较高、硬度较大等特点 |
NA为阿伏加德罗常数,下列说法正确的是
| A.某温度时,pH = 6的纯水,含10-6NA个OH- |
| B.含10.6 g Na2CO3的溶液中,所含阴离子总数等于0.1NA |
| C.V L a mol/L的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目大于3NA |
| D.工业用电解法进行粗铜精炼时,每转移1 mol电子,阳极上溶解的铜原子数必为0.5NA |
化学用语是学习化学重要工具,下列化学用语中,书写不正确的是
A.CH3COOH在水中的电离:CH3COOH CH3COO— + H+ CH3COO— + H+ |
B.碳酸氢钠的水解:HCO3— + H2O  CO32- + H3O+ CO32- + H3O+ |
C.电解硝酸银溶液:4Ag+ + 2H2O  4Ag + 4 H+ + O2↑ 4Ag + 4 H+ + O2↑ |
| D.向含有硫酸钙的水垢中加入碳酸钠溶液,沉淀的转化可表示为: |
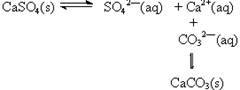
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中不正确的是
| A.由Al、Cu、稀H2SO4组成原电池,负极反应式为:Al - 3eˉ=Al3+ |
| B.由Fe、Cu、FeCl3溶液组成原电池,正极反应式为:2Fe3+ + 2eˉ=2Fe2+ |
| C.由Mg、Al、NaOH溶液组成原电池,负极反应式为:Al - 3eˉ+ 3OHˉ=Al(OH)3 |
| D.由Al、Cu、浓硝酸组成原电池,正极反应式为:4H+ + 2NO3- + 2eˉ=2NO2 + 2H2O |
有两位希腊化学家,把氢气和氮气通入到一加热的电解池中,用多孔钯多晶薄膜催化电解,结果在常压下获得了氨,且转化率远高于通常合成氨工艺的转化率。则下列有关叙述不正确的是
| A.在该装置内,氮气在阴极区发生反应 |
| B.使用高效催化剂可提高合成氨的转化率 |
| C.该过程中有电能转化为化学能 |
| D.合成氨反应是放热的,所以该装置还可以向外界提供能量 |
已知H—H键能为436 kJ/mol,H—N键能为391 kJ/mol,根据热化学方程式:
N2 (g)+ 3H2(g) 2NH3(g)ΔH =" -92.4" kJ/mol,则N≡N键的键能是
2NH3(g)ΔH =" -92.4" kJ/mol,则N≡N键的键能是
| A.431 kJ/mol | B.946 kJ/mol | C.649 kJ/mol | D.869 kJ/mol |