下列是一些化学键的键能。
| 化学键 |
C—H |
C—F |
H—F |
F—F |
键能/(kJ·mol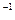 ) ) |
414 |
489 |
565 |
155 |
根据键能数据估算CH4 (g)+4F2 (g) =CF4(g) +4HF(g) 的反应热ΔH为
| A.–1940 kJ · mol-1 | B.1940 kJ · mol-1 | C.–485 kJ · mol-1 | D.485 kJ · mol-1 |
下列离子方程式的书写正确的是()
| A.铁和稀硫酸反应:2Fe + 6H+ =2Fe 3+ +3H2↑ |
| B.NaHCO3溶液与NaOH溶液反应: OH- + HCO3- = CO32― + H2O |
| C.钠和冷水反应Na+2H2O=Na++2OH-+H2↑ |
| D.氯化铝溶液中加入过量的氨水 Al3+ + 4NH3·H2O =AlO2- + 4NH4++ 2H2O |
把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的浓度恰好相等。则已反应的Fe3+和未反应的Fe3+的物质的量之比为()
| A.1:1 | B.1:2 | C.2:3 | D.3:2 |
少量的钠暴露在空气中,最终产物是()
| A.NaOH | B.Na2CO3·10H2O | C.Na2CO3 | D.NaHCO3 |
实验室制备Al(OH)3最好用()
| A.Al2O3和稀盐酸 | B.Al2O3和水 |
| C.AlCl3 和氨水 | D.Al2(SO4)2和KOH |
下列描述的一定是金属元素的是()
| A.原子核内有11个质子的元素 |
| B.能与酸反应的物质 |
| C.原子的最外层只有1个电子的元素 |
| D.易失去电子的物质 |