已知下列两个热化学方程式
2H2(g)+ O2(g)= 2H2O(l);△H=-571.6kJ/mol
C3H8(g)+ 5O2(g)= 3CO2(g)+4H2O(l);△H=-2220 kJ/mol
实验测得氢气和丙烷气体共5mol完全燃烧放热3847kJ,则混合气体中氢气与丙烷的体积比是( )
| A.1︰3 | B.3︰1 | C.1︰4 | D.1︰1 |
碘值是指100 g油脂中所能吸收(加成)碘的克数。测得某植物油碘值为a g,以NA表示阿伏加德罗常数,则b g该植物油中含有的碳碳双键数为
| A.abNA/25400 | B.abNA/12700 | C.abNA/2.54 | D.abNA/1.27 |
取Na2O、Na2O2、Na2CO3的固体混合物做了以下实验,以下记录不符合事实的是
| A.加入水中,产生无色气体 |
| B.加入酚酞溶液中,溶液先变红后褪色 |
| C.在干空气中加热到400℃,质量减少 |
| D.与SO2反应后,检测到有Na2SO4生成 |
下列有机反应在酸、碱性条件下都能进行的是
| A.银镜反应 | B.乙醇脱水 |
| C.油脂水解 | D.溴乙烷水解 |
以下工业上或实验室里催化剂的使用不符合事实的是
| A.氨氧化-三氧化二铬 | B.乙醇氧化-铜 |
| C.合成氨-铁触媒 | D.二氧化硫氧化-铂铑合金 |
实验室常用全是磨砂接口的曲颈甑制取HNO3(如图),反应的化学方程式为:NaNO3+H2SO4 NaHSO4+HNO3↑用曲颈甑是因为HNO3
NaHSO4+HNO3↑用曲颈甑是因为HNO3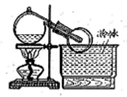
| A.会腐蚀橡胶 | B.易挥发 |
| C.易分解 | D.是强电解质 |