六氟化硫分子为正八面体构型(分子结构如图所示),难溶于水,在高温下仍有良好的绝缘性,在电器工业方面具有广泛用途。下列推测正确的是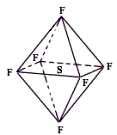
| A.SF6中各原子均达到8电子稳定结构 |
| B.SF6易燃烧生成SO2 |
| C.SF6分子是含有极性键的非极性分子 |
| D.SF6的一氯代物只有一种 |
下列有关物质的制备和转化正确的是
| A.常温下,用铝与浓硫酸反应制备二氧化硫 |
| B.氯化钡溶液中通入二氧化硫可生成BaSO3沉淀 |
| C.用FeS除去废水中的重金属铜离子 |
| D.以粗铜作阴极,硫酸铜溶液为电解质溶液电解精炼铜 |
下列有关溶液的存储和配置的描述错误的是
| A.新制的氯水可盛放在棕色细口瓶中 |
| B.水玻璃可存放在橡胶塞的细口瓶中 |
| C.配置FeCl3溶液,先加浓盐酸溶液溶解氯化铁固体,再稀释至相应浓度 |
| D.称取2.5g硫酸铜晶体,加100ml水溶液配制0.1mol.L—1硫酸铜溶液 |
下列涉及化学概念和进本原理说法正确的是
| A.12C14C C60互为同分异构体 |
| B.由同种元素组成的物质一定是纯净物 |
| C.金属氧化物存在酸性氧化物 |
| D.N2O3的水溶液能导电,说明N2O3是电解质 |
下列与摩尔盐[(NH4)2Fe(SO4)2.6H2O溶液有关离子方程式错误的是
| A.通入足量的溴水:2Fe2++Br2=2Fe3++2Br- |
| B.先加盐酸在通入BaCl2溶液:SO42-+Ba2+=BaSO4↓ |
| C.加氢氧化钠固体加热:NH4++OH-=NH3↑+H2O |
| D.检验该溶液是否变质:Fe3++3SCN-=Fe(SCN)3 |
化学反应条件(浓度、温度、加入实际量或顺序等)的变化会影响化学反应结果。下列对产生不同化学反应结果的影响因素分析错误的是
| 选项 |
反应物质 |
反应结果 |
影响因素 |
| A |
Na O2 |
Na2O Na2O2 |
反应温度 |
| B |
Cu HNO3 |
NO NO2 |
铜的还原性 |
| C |
Na2S溶液 SO2 |
澄清或者浑浊 |
SO2通入量 |
| D |
AgNO3 NH3.H2O |
澄清或者浑浊 |
试剂加入顺序 |