对于mA(s) + nB(g)  eC(g) + f D(g),反应过程中,当其它条件不变时,C的百分含量(C%)和压强(P)的关系如图,下列叙述正确的是
eC(g) + f D(g),反应过程中,当其它条件不变时,C的百分含量(C%)和压强(P)的关系如图,下列叙述正确的是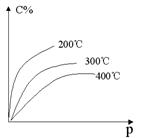
| A.达到平衡后,加入催化剂,则C%增大 |
| B.达到平衡后,若升温,平衡逆向移动 |
| C.化学方程式中n<e +f |
| D.达到平衡后,增加A的量,平衡正向移动 |
下列反应中属于消去反应的是( )
| A.乙烯使溴水褪色 |
| B.乙醇与浓硫酸共热至170℃ |
| C.溴乙烷与NaOH水溶液共热 |
| D.在液溴与苯的混合物中撒入铁粉 |
下列5种烃:①2-甲基丙烷;②乙烷;③丙烷;④丁烷;⑤戊烷。按它们的沸点由高到低的顺序排列正确的是( )
| A.①②③④⑤ | B.⑤④①③② |
| C.④⑤②①③ | D.③①②⑤④ |
用于制造隐形飞机的某种物质,具有吸收微波的功能,其主要成份的分子结构如下图所示,它 属于( ) 
| A.新型无机非金属材料 | B.无机化合物 |
| C.有机高分子化合物 | D.有机物 |
甲~辛等元素在周期表中的位置如下表所示。下列说法正确的是
| A.甲、丁、戊的单质都是金属 |
| B.乙、丙、辛都是非金属元素 |
| C.乙、庚、辛都能形成氧化物 |
| D.已的氧化物既可溶于KOH溶液又可溶于H2SO4溶液 |
下列有机化合物中,属于烃的有
| A.CH3CH3 | B.CH2=CHCH3 |
| C.CH3CH2OH | D.CH3CH2 COOH |