已知NaHSO4在水中的电离方程式为:NaHSO4==Na++H++SO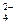 。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是( )
。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是( )
| A.该温度高于25℃ |
| B.由水电离出来的H+的浓度是1.0×10-12mol·L-1 |
| C.加入NaHSO4晶体抑制了水的电离 |
| D.该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性 |
不能说明X的电负性比Y的电负性大的是()。
| A.与H2化合时X单质比Y单质容易 |
| B.X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强 |
| C.X原子的最外层电子数比Y原子最外层电子数多 |
| D.X单质可以把Y从其氢化物中置换出来 |
元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。下列推测不正确的是 ()。
| A.同周期元素中X的金属性最强 |
| B.原子半径X>Y,离子半径X+>Z2- |
| C.同族元素中Z的氢化物稳定性最高 |
| D.同周期元素中Y的最高价含氧酸的酸性最强 |
价电子排布式为2s22p5的元素,下列有关它的描述正确的有()。
| A.原子序数为7 | B.电负性最大 |
| C.原子半径最大 | D.第一电离能最大 |
下列关于元素的电负性大小的比较中,不正确的是()。
| A.O<S<Se<Te | B.C<N<O<F |
| C.P<S<O<F | D.K<Na<Mg<Al |
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是()。
| A.X与Y形成化合物时,X可以显负价,Y显正价 |
| B.第一电离能Y一定小于X |
| C.最高价含氧酸的酸性:X对应的含氧酸的酸性弱于Y对应的含氧酸的酸性 |
| D.X元素气态氢化物的稳定性大于Y元素气态氢化物的稳定性 |