下列原子序数所对应的元素组中,两者可形成离子键的是
| A.1和17 | B.12和9 | C.14和6 | D.15和8 |
下图是课外活动小组设计的用化学电源使LED灯发光的装置。下列说法错误的是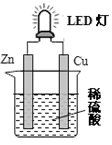
| A.铜片表面有气泡生成 |
| B.装置中存在“化学能→ 电能→ 光能”的转换 |
| C.如果将硫酸换成柠檬汁,导线中不会有电子流动 |
| D.如果将锌片换成铁片,电路中的电流方向不变 |
下列表示反应是吸热反应的是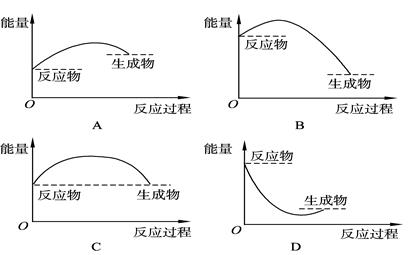
可逆反应A(g)+3B(g) 2C(g)+2D(g)在4种不同情况下反应速率分别如下,其中反应速率最大的是
2C(g)+2D(g)在4种不同情况下反应速率分别如下,其中反应速率最大的是
A.v(A)=0.15mol/(L·min)B.v (B)=0.3 mol/(L·min)
C.v (C)=0.2 mol/(L·min) D.v (D)=0.1 mol/(L·min)
在一定温度下,可逆反应X(g)+3Y(g) 2Z(g)达到平衡的标志是
2Z(g)达到平衡的标志是
| A.X生成的速率与Z分解的速率相等 |
| B.单位时间生成a mol X,同时生成3a mol Y |
| C.X、Y、Z的分子数比为1∶3∶2 |
| D.X、Y、Z的浓度不再变化 |
一定条件下,CO和CH4燃烧的热化学方程式为:2CO(g)+O2(g) 2CO2(g) ΔH=-566kJ/mol
2CO2(g) ΔH=-566kJ/mol
CH4(g) +2O2(g) CO2(g)+2H2O(l);ΔH=-890kJ/mol ,1molCO和3mol CH4组成的混合气在上述条件下完全燃烧时,释放的热量为
CO2(g)+2H2O(l);ΔH=-890kJ/mol ,1molCO和3mol CH4组成的混合气在上述条件下完全燃烧时,释放的热量为
| A.2 912 kJ | B.2 953 kJ | C.3 236 kJ | D.3 867 kJ |