为了研究化学反应X+Y=Z的能量变化情况,某同学设计了下图所示装置。当向盛有X的试管中滚圆试剂Y时,看到U型管中甲处液面下降乙处液面上升,由此说明:
①反应为放热反应
②生成物的总能量比反应物的总能量高
③物质中的化学能通过化学反应转化成热能释放出来
④反应物化学键断裂吸收的能量高于生成物化学键形成放出的能量
| A.①② | B.①③ | C.①②③ | D.②③④ |
30、2N2O5(g)=4NO2(g)+O2(g) △H=+56.8kJ/mol自发进行的原因是
| A.是吸热反应; |
| B.是放热反应; |
| C.是熵减少的反应; |
| D.熵增大效应大于能量效应。 |
29.下列说法正确的是
| A.某反应低温条件下能自发进行,那么高温条件也一定能自发进行 |
| B.某反应高温条件下不能自发进行,那么低温条件也不能自发进行 |
| C.反应方向是由焓变和熵变共同决定的,与反应温度无关 |
| D.温度有可能对反应的方向起决定性的作用 |
28.在一定温度不同压强(P1<P2)下,可逆反应2X(g)2Y(g) + Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是
27.下图中的曲线是表示其他条件一定时,2NO+O2 2NO2 △H<0 ,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是
2NO2 △H<0 ,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是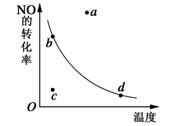

| A.a点 | B.b点 | C.c点 | D.d点 |
26.在恒温时,一固定容积的容器内发生如下反应:2NO2(g)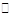 N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数
N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数
| A.减小 | B.增大 | C.不变 | D.无法判断 |