德国科学家格哈德 · 埃特尔对有关一氧化碳在金属铂表面的氧化过程的研究,催生了汽车尾气净化装置。净化装置中的催化转化器,可将CO、NO、NO2和碳氢化合物等转化为无害的物质,有效降低尾气对环境的危害。下列有关说法不正确的是( )
| A.催化转化器中的铂催化剂可加快CO氧化 |
| B.在铂催化下,NO、NO2可被CO还原成N2 |
| C.碳氢化合物在铂催化下,被CO直接氧化成CO2和H2O |
| D.铂表面做成蜂窝状更有利于提高催化效果 |
下列判断合理的是( )
①等物质的量的NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后生成CO2的质量相等
②根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③根据电解质在熔融状态下能否完全电离将电解质分为强电解质和弱电解质
④根据元素原子最外层电子数的多少将元素分为金属和非金属
⑤根据反应的热效应将化学反应分为放热反应和吸热反应
⑥合金的熔点通常比组分金属高,硬度比组分金属大
| A.只有②⑥ | B.只有②⑤ | C.只有①②⑤⑥ | D.只有②③④⑤ |
Na2SO4溶液的溶解度曲线如图,下列说法一定正确的是()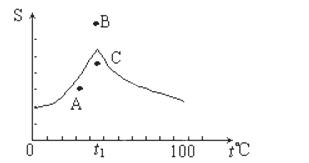
A.A点表示Na2SO4溶液尚未达到饱和,但降温和加入Na2SO4·H2O晶体都可使其饱和
B.B、C点表示t1℃时,Na2SO4溶液在B点的溶解度大于在C点的溶解度
C.在C点时Na2SO4溶液降温或升温,都会使其溶液变澄清
D.制取芒硝的最佳方法是在100℃时配成饱和溶液,再降温至0℃析出晶体
某温度下,氯化镁饱和溶液浓度为40%,在足量的此溶液中加入4.6g无水氯化镁,最终析出结晶水合物40.6g,则该结晶水合物的化学式是()
| A.MgCl2·7H2O | B.MgCl2·2H2O | C.MgCl2·6H2O | D.MgCl2·5H2O |
将氯气通入一定温度的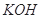 溶液中,得到含有次氯酸钾、氯酸钾和氯化钾的混合溶液。若反应过程中转移
溶液中,得到含有次氯酸钾、氯酸钾和氯化钾的混合溶液。若反应过程中转移 个电子,所得溶液中
个电子,所得溶液中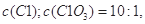 则参与反应的
则参与反应的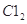 的物质的量为
的物质的量为
A. |
B.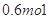 |
C.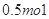 |
D.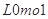 |
历史上最早应用的还原性染料是靛蓝,其结构简式如图所示,下列关于靛蓝的叙述中错误的是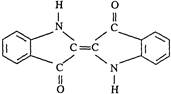
| A.靛蓝由碳、氢、氧、氮四种元素组成 |
| B.它的分子式是C16H10N2O2 |
| C.该物质是高分子化合物 |
| D.它是不饱和的有机物 |