目前在水的净化处理、纸浆的加工等化学工艺中普遍用到一种高分子化合物聚丙烯酰胺。它可由化合物A(分子式C3H6)经以下反应流程制得: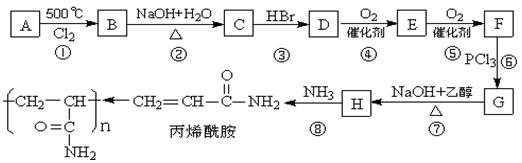
已知:(1)3RCOOH+PCl3 3RCOCl+H3PO3
3RCOCl+H3PO3
(2)RCOCl+NH3 RCONH2+HCl
RCONH2+HCl
试回答下列问题:
(1)写出A和H的结构简式A ,H 。
(2)关于丙烯酰胺的下列叙述中正确的是: 。
| A.能使酸性KMnO4溶液褪色; | B.能发生加聚反应生成高分子化合物; |
| C.与α—氨基乙酸互为同系物; | D.能与H2发生加成反应 |
(3)写出D→E的反应方程式: 。
(4)C→D的目的是 。
(5)上述反应过程中属于取代反应的是: 。
(6)丙烯酰胺有多种同分异构体,同时符合下列要求的同分异构体有多种:
①链状,无碳碳叁键; ②同一个碳原子上不能连有2个双键。
试写出其中的2种的结构简式: 、 。
(4分)有下列物质:①空气 ②O2 ③NaHSO4 ④氨水 ⑤CuSO4·5H2O ⑥NaOH
⑦CO2 ⑧Fe2O3 ⑨金刚石 ⑩H2SO4 ,请回答下列问题(请在横线上填写序号):
(1)属于混合物的有;
(2)属于酸性氧化物的有;
(3)属于碱的有;
(4)属于盐的有。
(14分)氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
依据上图,完成下列填空:
(1)在电解过程中电解池中所发生总反应的离子方程式为:________,与电源负极相连的电极附近,溶液PH ________。(选填“不变”“升高”或“下降”)
(2)工业食盐中含Ca2+、Mg2+等杂质。精制过程中发生的离子方程式为、。
(3)若粗盐中SO42—含量较高,必须添加钡试剂除去SO42—,该钡试剂可以是 ;
a、Ba(OH)2 b、Ba(NO3)2 c、BaCl2
(4)为了有效除去Ca2+、Mg2+、SO42—,加入试剂的合理顺序为 ;
a、先加NaOH,后加Na2CO3,再加钡试剂
b、先加NaOH,后加钡试剂,再加Na2CO3
c、先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过 、冷却、 。(填操作名称)除去NaCl。
(10分)电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。
请回答以下问题:
⑴若X、Y都是惰性电极,a是饱和CuCl2溶液,则
①电解池中X极上的电极反应式是________;
②Y电极上的电极反应式是________;检验该电极反应产物的方法是________。
⑵如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①Y电极的材料是________;
②假若电路中有0.04摩尔电子通过时,阴极增重________克。
(9分)根据下列氧化还原反应2FeCl3+Cu===2FeCl2+CuCl2设计一个原电池: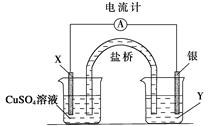
请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是________;
(2)银电极为电池的________极,发生的电极反应为_________________________;
X电极上发生的电极反应为_________________________;
(3)外电路中的电子是从________电极流向________电极(填具体电极如Ag”)。
(10分)如图所示,水槽中试管内有一枚铁钉,放置数天观察:
(1)铁钉在逐渐生绣。
(2)若试管内液面上升,发生 腐蚀,电极反应:负极:,正极:。
(3)若试管内液面下降,则原溶液呈性,发生的电极反应:正极:。