(1)能源是当今社会发展的三大支柱之一。天然气是一种高效、低耗、污染小的清洁能源,主要成分为甲烷,甲烷燃烧的化学方程式为: ;
; 标准状况下,11.2L甲烷燃烧时,转移电子的物质的量为 mol。
标准状况下,11.2L甲烷燃烧时,转移电子的物质的量为 mol。

 s
s
 在如图构想的物质循环中太阳能最终转化为 能。
在如图构想的物质循环中太阳能最终转化为 能。
 (2)钢铁的腐蚀现象非常普遍,电化学腐蚀是造成钢铁腐蚀
(2)钢铁的腐蚀现象非常普遍,电化学腐蚀是造成钢铁腐蚀 的主要原因,某同学按右图进行钢铁腐蚀的模拟,则
的主要原因,某同学按右图进行钢铁腐蚀的模拟,则
负极的电
 极反应式为 ,
极反应式为 , 正极的电极反应式为 。
正极的电极反应式为 。 【提示:电化学的总反应式为2Fe+2H2O+O2=2Fe(OH)2】
【提示:电化学的总反应式为2Fe+2H2O+O2=2Fe(OH)2】 (3)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:
(3)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:

 操作①的名称是 ;反应②的离子方程式是 ,下述物质中不可做试剂③的是 。
操作①的名称是 ;反应②的离子方程式是 ,下述物质中不可做试剂③的是 。
| A.乙醇 | B.苯 | C.乙酸 | D.四氯化碳 |
火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+C+S===K2S+2NO2↑+CO2↑。
(1) 其中被氧化的元素是,还原产物是(填符号)。
(2) 当该反应生成6.72 L CO2(标况下)时,氧化剂一共得到mol电子。
(8分)某工厂的工业废水中含有大量的FeS O4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝
O4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝 ,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,填写物质名称(或主要成分的化学式)或操作方法,完成回收硫酸亚铁和铜的简单实验方案。
,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,填写物质名称(或主要成分的化学式)或操作方法,完成回收硫酸亚铁和铜的简单实验方案。
(1)A是, E是;
(2)操作Ⅱ是,操作Ⅲ是。
(14分) “洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了热值高达122500~16000 kJ·m-3的煤炭气,其主要成分是CO和H2。CO和H2可作为能源和化工原料,应用十分广泛。
(1)已知:
C(s)+O2(g)=CO2(g) ΔH1=—393.5 kJ·mol-1 ①
2H2(g)+O2(g)=2H2O(g) ΔH2=—483.6 kJ·mol-1 ②
C(s)+H2O(g)=CO(g)+H2(g) ΔH3=+131.3 kJ·mol-1 ③
则反应CO(g)+H2(g) +O2(g)= H2O(g)+CO2(g),ΔH= kJ·mol-1。标准状况下的煤炭气(CO、H2)33.6 L与氧气完全反应生成CO2和H2O,反应过程中转移 mol e-。
(2)工作温度650℃的熔融盐燃料电池,是用煤炭气(CO、H2)作负极燃气,空气与CO2的混合气体在正极反应,用一定比例的Li2CO3和Na2CO3低熔点混合物做电解质,以金属镍(燃料极)为催化剂制成的。负极的电极反应式为:CO+H2-4e-+2CO32-=3CO2+H2O;则该电池的正极反应式为 。
(3)密闭容器中充有10 mol CO与20 mol H2,在催化剂作用下反应生成甲醇:CO(g)+2H2(g)  CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如右图所示。
CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如右图所示。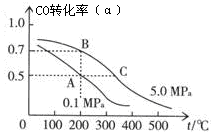
①若A、B两点表示在某时刻达到的平衡状态,此时在A点时容器的体积为VAL,则该温度下的平衡常数K= ;A、B两点时容器中物质的物质的量之比为n(A)总:n(B)总= 。
②若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA tC(填“大于”、“小于”或“等于”)。
③在不改变反应物用量的情况下,为提高CO的转化率可采取的措施是 。
A 降温 B 加压 C 使用催化剂 D 将甲醇从混合体系中分离出来
写出戊烷的所有同分异构体的结构简式并用系统命名法命名:
,
其一氯代物的同分异构体共有种。
(12分)化工厂生产的某产品只含C、H、O三种元素,分子模型如下图所示(图中球与球之间的连线代表化学键,如单键、双键等)。
(1)该产品的结构简式为_______,所含官能团的名称:_____________
(2)该有机物的核磁共振氢谱上有________个峰(信号)
(3)下列物质中,与该产品互为同分异构体的是_____________(填序号,下同)与该产品
互为同系物的是_____________。
①CH3CH="CHCOOH" ②CH2=CHCOOCH3 ③CH3CH2CH=CHCOOH ④CH3CH(CH3)COOH