(1)下表为烯类化合物与溴发生加成反应的相对速率。(以乙烯为标准)
| 烯类化合物 |
相对速率 |
| (CH3)2C |
10.4 |
| CH2CH |
2.03 |
| CH2 |
1.00 |
| CH2 |
0.04 |
据表中数据,总结烯类化合物加溴时,反应速率与C C上取代基的种类、个数间
的关系: 。
(2)下列化合物与氯化氢加成时,取代基对速率的影响与上述规律类似,其中反应速率
最慢的是 (填代号)
| A.(CH3)2C |
B.CH3CH |
| C.CH2 |
D.CH2 |
(3)已知:①下列框图中B的结构简式为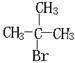 ;
; ;
; 其中部分反应条件、试剂被省略。
其中部分反应条件、试剂被省略。
 |
试回答下列问题:
(1)分别写出A 和D的结构简式  , ;
, ;
(2)反应②的化学方程式为 ,反应类型为 。
(3)写出C物质的一种同系物 。
(4)写出A的另一种同分异构体的结构简式 。
实验室制备少量硫酸亚铁晶体的实验步骤如下:取过量洁净的铁屑,加入20%~30%的稀硫酸溶液,在50℃~80℃水浴中加热至不再产生气泡.将溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口、静置、冷却一段时间后有浅绿色晶体析出,收集产品。
(1)写出该实验制备硫酸亚铁的化学方程式: ;
(2)采用水浴加热的原因是 ;
(3)反应时铁屑过量的目的是(用离子方程式表示);
(4)溶液趁热过滤的原因是 ;
(5)塞紧试管口的目的是。
在实验室里可用右图所示装置来制取氯酸钠、次氯酸钠和探究氯水的性质。图中:
①为氯气发生装置;②的试管里盛有15 mL 30% NaOH溶液来制取氯酸钠,并置于热水浴中;
③的试管里盛有15 mL 8% NaOH溶液来制取次氯酸钠,并置于冰水浴中;
④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验室制Cl2的化学方程式;
实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有_______(填写下列编号字母)的净化装置。
| A.碱石灰 | B.氢氧化钠溶液 | C.饱和食盐水 | D.浓硫酸 |
(2)如果将过量二氧化锰与20 mL 12 mol·L-1的浓盐酸混合加热,充分反应后生成的氯气0.06 mol。(填“大于” “小于” “等于”),若有17.4g的MnO2被还原,则被氧化的HCl质量为。
(3)比较制取氯酸钠和次氯酸钠的条件,二者的差异是
①;②。
(4) 实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白。
| 实验现象 |
原因 |
| 溶液最初从紫色逐渐变为红色 |
氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 |
______________________________________ |
| 然后溶液从无色逐渐变为_______色 |
______________________________________ |
欲配制480mL 0.2mol/L的NaCl溶液,回答下列问题:
(1)应用托盘天平准确称取固体NaCl g。
(2)以下是实验操作步骤,正确的操作顺序是:
①称取所需质量的NaCl
②将溶液转移到容量瓶内
③用蒸馏水洗涤烧杯2~3次,将洗涤液全部移入容量瓶中,摇匀
④改用胶头滴管,小心滴入蒸馏水至刻度
⑤仔细地把蒸馏水注入容量瓶中,直到液面接近刻度线1cm~2cm处
⑥塞上瓶塞,反复上下颠倒,摇匀
⑦将称取的NaCl固体,加适量蒸馏水,搅拌溶解后冷却
(3)若实验遇到下列情况,所配制的溶液浓度偏小的操作是
| A.烧杯中NaCl溶液移入容量瓶后没有洗涤烧杯 |
| B.定容后摇匀,发现液面低于刻度线,再滴加蒸馏水至刻度线 |
| C.实验用的容量瓶洗净后未干燥,里面含有少量水 |
| D.定容时俯视 |
下图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:。
装置B中饱和食盐水的作用是;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入。
| a |
b |
c |
d |
|
| Ⅰ |
干燥的有色布条 |
干燥的有色布条 |
湿润的有色布条 |
湿润的有色布条 |
| Ⅱ |
碱石灰 |
硅胶 |
浓硫酸 |
无水氯化钙 |
| Ⅲ |
湿润的有色布条 |
湿润的有色布条 |
干燥的有色布条 |
干燥的有色布条 |
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为色,打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是。
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的化学方程式:。
某同学购买了一瓶××牌“84消毒液”,查阅相关资料和消毒液包装说明得到如下信息:“84消毒液”:含25%NaClO 1 000 mL、密度1.19 g·cm-3。
请根据以上信息和相关知识回答下列问题:
(1)该“84消毒液”的物质的量浓度为mol·L-1(保留两位有效数字)。
(2)某实验需用480 mL含25%NaClO的消毒液。该同学参阅该“84消毒液”的配方,欲用NaClO固体配制该消毒液。
①下列说法正确的是。
A.如上图所示的仪器中,有四种是不需要的,还需一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干才能用于溶液配制
C.利用久置的NaClO来配制可能导致结果偏低
D.需要称量的NaClO固体质量为143 g
②在配制过程中,下列操作可能使配制的溶液的浓度偏大的是。
A.烧杯中溶液转移到容量瓶中时,未洗涤烧杯
B.定容时,俯视刻度线
C.定容时,仰视刻度线
D.移液时,有少量液体溅出