右图为实验室制取少量乙酸乙酯的装置图。下列关于该实验的叙述中不正确的是( )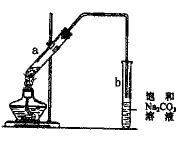
| A.向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加乙酸 |
| B.试管b中导气管下端管口不能浸入液面的目的是防止实验过程中产生倒吸现象 |
| C.制得的乙酸乙酯是一种无色透明、有香味的油状液体 |
| D.向a试管中加入几块碎瓷片的作用是防止加热时液体暴沸 |
制印刷电路时常用氯化铁溶液作为“腐蚀液”,发生的反应为2FeCl3+Cu===2FeCl2+CuCl2。向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
| A.烧杯中有铜无铁 | B.烧杯中有铁无铜 |
| C.烧杯中铁、铜都有 | D.烧杯中铁、铜都无 |
甲、乙、丙、丁分别是Al2(SO4)3、FeSO4、NaOH、BaCl2四种物质中的一种,若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失,丁溶液滴入甲溶液时,无明显现象发生,据此可推断丙物质是
| A.Al2(SO4)3 | B.NaOH | C.BaCl2 | D.FeSO4 |
在氯化铁、氯化铜和盐酸混合溶液中加入铁粉,待反应结束,所剩余的固体滤出后能被磁铁吸引,则反应后溶液中存在较多的阳离子是
| A.Cu2+ | B.Fe3+ | C.Fe2+ | D.H+ |
镭是元素周期表中第ⅡA族元素,下列关于镭的叙述不正确的是
| A.镭比钙的金属性更强 | B.在化合物中呈+2价 |
| C.镭是一种放射性元素 | D.氢氧化镭呈两性 |
某些化学试剂可用于净水。水处理中使用的一种无机高分子凝聚剂的化学式可表示为[Al2(OH)nClm·yH2O]x,式中m等于
| A.3-n | B.6-n | C.6+n | D.3+n |