X、Y两种元素的原子的质子数之和为20,两元素形成的化合物在水溶液中能电离出电子层结构相同的阴阳离子,则X、Y形成的化合物是 (  )
)
| A.MgF:z | B.NaF | C.LiCl | D.Na2O |
下列依据相关实验得出的结论正确的()
| A.SiO2既能与HF溶液反应,又能与NaOH溶液反应,说明SiO2是两性氧化物 |
| B.用大理石和浓盐酸反应制取CO2气体,立即通入一定浓度的Na2SiO3溶液中,出现白色沉淀证明H2CO3的酸性比H2SiO3的酸性强 |
| C.向某溶液中滴加硝酸酸化的Ba(NO3)2溶液产生白色沉淀,说明该溶液中含有SO42- |
| D.相同体积PH均为3的HA和HB两种酸分别与足量的锌充分反应,HA放出的氢气多,说明HB的酸性比HA的酸性强 |
混合下列各组物质使之充分反应,加热蒸干产物并高温下灼烧至质量不变,最终残留固体为纯净物的是()
| A.向CuSO4溶液中加入适量铁粉 |
| B.等物质的量浓度、等体积的FeCl3与KI溶液混合 |
| C.物质的量之比为2:1的NaHCO3与Na2O2溶于水 |
| D.在Na2SiO3溶液中通入过量CO2气体 |
碱性电池具有容量大,放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn+2MnO2+2H2O=Zn(OH)2+2MnOOH,下列说法错误的是()
| A.电池工作时,锌失去电子 |
| B.电池正极的电极反应式为:2MnO2+2H2O+2e-=2MnOOH+2OH- |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2 mol 电子,锌的质量理论上减少6.5 g |
已知: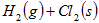
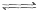
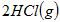 △
△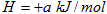
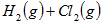
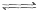
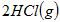 △
△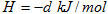
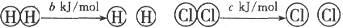 ,
,
且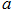 、
、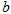 、
、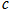 、
、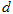 均大于零,则下列说法正确的是()
均大于零,则下列说法正确的是()
A.断开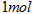 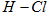 键所需的能量为 键所需的能量为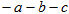 |
B.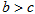 ,则氢气分子具有的能量高于氯气分子具有的能量 ,则氢气分子具有的能量高于氯气分子具有的能量 |
C.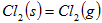 △ △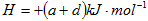 |
D.向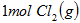 中通入 中通入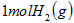 ,发生反应时放热 ,发生反应时放热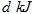 |
下列离子方程式正确的是()
| A.0.01mol/L NH4Al(SO4)2溶液与0.01mol/L Ba(OH)2溶液等体积混合 NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O |
| B.Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O |
| C.将11.2L标准状况下的氯气通入200mL2mol/L的FeBr2溶液中,离子反应方程式为: 4Fe2++6Br-+5Cl2= 4Fe3++3Br2+10Cl- |
| D.铁粉中滴加少量浓硝酸:Fe+3NO3-+6H+= Fe3++3NO2↑+3H2O |