在容积一定的密闭容器中发生可逆反应A(g)+2B(g)  2C(g)-Q,平衡移动关系如图所示。下列说法正确的是
2C(g)-Q,平衡移动关系如图所示。下列说法正确的是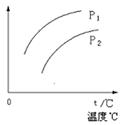
| A.P1>P2,纵坐标指A的质量分数 |
| B.P1> P2,纵坐标指C的质量分数 |
| C.P1< P2,纵坐标指A的转化率 |
| D.P1< P2,纵坐标指混合气体的平均摩尔质量 |
有A、B、C、D四种一元酸溶液,对它们进行的有关实验及其结果分别为:(1)在物质的量浓度相同的A、C两溶液中,都滴加几滴甲基橙时,A溶液呈黄色,C溶液呈橙色(2)B的钠盐溶液的pH值小于C的钠盐溶液pH值(3)A酸与D的盐反应生成A的盐和D酸。由此可以确定这四种酸的酸性由强到弱的正确排列顺序为 ()
A.B>C>A>D B.A>C>B>D C.D>A>C>B D.C>B>A>D
某温度下,100 mL 0.4 mol/L醋酸溶液与足量Zn粒反应生成H2的速率v(H2)=0.01mol/(L·min)。下列有关说法正确的是()
| A.为了减缓反应速率,但又不影响生成H2的总量,可向该溶液中加入少量CaCO3固体 |
| B.为了减缓反应速率,但又不影响生成H2的总量,可向该溶液中加入10 mL 0.1 mol/L醋酸溶液 |
| C.为了减缓反应速率,但又不影响生成H2的总量,可向该溶液中加入少量NaNO3溶液 |
| D.若向该溶液中加入少量醋酸钠固体,反应速率可能变成v(H2)="0.3" mol/(L·h) |
常温下,下列溶液中可能大量共存的离子组是()
| A.加入金属镁能产生大量H2的溶液中:Na+、NH4+、F-、SO32- |
| B.含有大量S2-的溶液中:H+、K+、Mg2+、NO3-、 |
| C.含有Al3+的溶液中:NH4+、Na+、SiO32-、HCO3- |
| D.水电离产生的c(OH-)=1×10-10 mol/L的溶液中:Al3+、SO42-、NO3-、Cl- |
由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,c(Al3+)=0.4mol·L-1,c(SO42-)=0.8mol·L-1,则c(K+)为( )
| A.0.15 mol·L-1 | B.0.2 mol·L-1 | C.0.3 mol·L-1 | D.0.4 mol·L-1 |
下列事实不能用勒夏特列原理解释的是()
| A.工业合成SO3的过程中使用过量的氧气,以提高二氧化硫的转化率。 |
| B.合成氨工厂通常采用20MPa~50MPa压强,以提高原料的利用率。 |
| C.在实验室里可用碳酸钙粉末和稀盐酸制得二氧化碳气体。 |
| D.实验室用排饱和食盐水的方法收集氯气。 |