a、b、c、d是四种短周期元素。a、b、d同周期,c、d同主族。a的原子结构示意图为: ,b与c形成化合物的电子式为:
,b与c形成化合物的电子式为: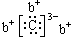 ,下列比较中正确的是()
,下列比较中正确的是()
| A.原子半径a>c>b | B.原子的氧化性a>c>d |
| C.最高价氧化物的熔点a>d>b | D.最高价含氧酸的酸性c>d>a |
能正确表示下列反应的离子方程式的是()
| A.碳酸氢钠溶液中加入硫酸氢钠溶液: CO32-+H+= CO2↑+H2O |
| B.硫化氢气体通入醋酸铅溶液: Pb2++H2S=PbS↓+2H+ |
| C.碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++2HCO3-+2OH-= CaCO3↓+CO32-+2H2O |
| D.磷酸二氢钠溶液中加入过量氢氧化钡溶液:2H2PO4-+4OH-+3Ba2+=Ba3(PO4)2↓+4H2O |
Inorganic Syntheses一书中,有一如图所示的装置,用以制备某种干燥的纯净气体。该装置中所装的药品正确的是()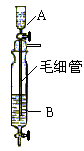
| A.A中装浓硫酸,B中装浓盐酸 |
| B.A中装浓盐酸,B中装浓硫酸 |
| C.A中装氢氧化钠浓溶液,B中装浓氨水 |
| D.A中装浓氨水,B中装氢氧化钠浓溶液 |
在含有FeBr2和FeI2的混合溶液中,通入过量的氯气,然后把溶液加热蒸干、灼烧,最后留下的是()
①FeCl2、②FeCl3、③I2、④Br2、⑤Fe(OH)3、⑥Fe2O3、⑦FeO。
| A.①③④ | B.③I2⑦ | C.③⑤ | D.⑥ |
向含下列微粒的溶液中,①HS-、②Fe2+、③ 、④
、④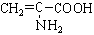 分别加入少量氢氧化钠固体,或少量浓盐酸或几滴酸性KMnO4溶液。(溶液体积变化忽略不计),都使溶液中对应的离子或分子浓度减少的是()
分别加入少量氢氧化钠固体,或少量浓盐酸或几滴酸性KMnO4溶液。(溶液体积变化忽略不计),都使溶液中对应的离子或分子浓度减少的是()
| A.①② | B.②③ | C.①④ | D.③④ |