盛有氯化钡稀溶液甲乙两试管分别通入SO2至饱和,若向甲试管中加入足量硝酸,乙试管中加入足量氢氧化钠溶液,则下列叙述正确的是( )
| A.甲、乙两试管都有白色沉淀生成 |
| B.甲、乙两试管都没有白色沉淀生成 |
| C.甲试管没有白色沉淀生成而乙试管有 |
| D.甲试管有白色沉淀生成而乙试管没有 |
设NA代表阿伏加德罗常数,下列说法中,正确的是()
| A.2.3g金属钠全部变成钠离子时失去的电子数目为0.2NA |
| B.2g氢气所含的原子数目为NA |
| C.17gNH3所含的电子数为10NA |
| D.NA个氧分子和NA个氢分子的质量比等于16∶1 |
元素X的离子结构示意图为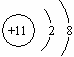 ,元素Y的原子结构示意图为
,元素Y的原子结构示意图为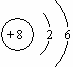 ,则X与Y形成的化合物的化学式为()
,则X与Y形成的化合物的化学式为()
| A.XY | B.X2Y | C.XY2 | D.X2Y2 |
关于容量瓶的四种叙述为:①是配制准确浓度溶液的仪器;②不宜贮藏溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中,正确的是()
| A.①②③④ | B.②③ | C.①②④ | D.②③④ |
下列叙述中,正确的是()
| A.一瓶溶液中各个部分的性质可能不同 |
| B.溶液一定是无色透明的混合物 |
| C.溶液和胶体中的分散质粒子均可以透过滤纸 |
| D.I2加入到CCl4中振荡可形成溶液 |
下列对物质属类的归纳中,错误的是()
| A.蔗糖、酒精、甲烷等这类含碳化合物属于有机物 |
| B.由金属离子和酸根离子组成的化合物称为盐 |
| C.在水溶液中电离出的阳离子全部为氢离子的化合物称为酸 |
| D.含氧元素的化合物称为氧化物 |