工业上生产硫酸时,利用催化氧化反应将转化为是一个关键步骤。压强及温度对转化率的影响如下表(原料气各成分的体积分数为: 7%, 11%, 82%):

(1)已知的氧化是放热反应,如何利用表中数据推断此结论?
(2)在400~500 ℃时,的催化氧化采用常压而不是高压,主要原因是:;
(3)选择适宜的催化剂,是否可以提高的转化率?(填"是"或"否"),是否可以增大该反应所放出的热量?(填"是"或"否");
(4)为提高吸收率,实际生产中用吸收;
(5)已知:,计算每生产1万吨98%硫酸所需要的质量和由生产这些所放出的热量。
(12分)关心父母是青少年的美德。学生小王为他患糖尿病的父母制作了一张食谱,为评价该食谱,他获得了下列资料。请阅读资料回答下列问题。
糖尿病原菌的致病原因之一是胰岛素缺乏。主要表现为血糖增高,合理的饮食是治疗糖尿病的基础,肥胖者要限制热量,减轻体重;消瘦者要有足够的热量以恢复理想的体重。饮食中碳水化合物所提供的热量不要高于总热量的55%—60%,胆固醇每日摄入量要低于300 mg,糖的食用要有节制。(资料来源:《中国大百科全书》)
专家对该类病人每日主要营养成分的推荐摄入量和上图食谱的实测数据如下表。
| 专家推荐摄入量 |
上图食谱实测数据 |
|
| 蛋白质(g) |
93 |
80 |
| 脂肪(g) |
70 |
50 |
| 碳水化合物(g) |
330 |
450 |
| 总热量(kJ) |
9 851 |
10 910 |
(1)已知每克蛋白质、脂肪、碳水化合物分别产生17 kJ、38 kJ、17 kJ热量;该食谱中蛋白质、脂肪和碳水化合物所提供的热量占总热量的百分比分别是:_________、_________和_________。
(2)通过对上题数据的分析,小王得到的结论是____________________________________。
(3)如果要对该食谱进行较为全面的分析,还需要的数据有__________________________。
(4)小王对食谱的评价过程包括,_________和_________得出结论等三个环节。
(6分)鲨鱼是世界上唯一不患癌症的动物,研究发现其体内含有的角鲨烯(分子式为C30H50)有抗癌作用。试计算:
(1)角鲨烯中碳、氢两元素的质量比_________;
(2)41 g角鲨烯与_________克水中所含的氢元素的质量相等?
(12分)2006年6月,我国海域发生2次红潮事件,这与洗涤剂的使用有关。通常洗涤剂中含有三磷酸五钠(Na5P3O10)。洗涤衣物的废水如直接排放到河湖中会造成水质富营养化,促使藻类大量繁殖,藻类死亡后经氧化,消耗水中的氧气,造成水中缺氧致使河水变黑变臭,鱼类等水生生物因缺氧而死亡。
(1)经测定知,某藻类的组成为:含C 35.76%,含O 49.50%,含N 6.310%,含H 7.370%,含P 0.870%,计算该藻类中各元素原子个数比(相对一个P原子) ________。
(2)藻类被氧气完全氧化的化学方程式(藻类用“化学式”表示,生成物除O外都为最高价化合物)为_____________________________。
(3)现有一个面积为1×106 m2、深20 m的湖泊,含氧量为9.1 g/m3,若每天排入3%(质量分数)三磷酸五钠的废水1 000 kg,多少天后湖里的氧气被耗尽(设空气中的氧气不再溶入湖水中)。
有以下四种物质:①22 g二氧化碳②8 g氢气③1.2×10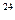 个氮气分子④4 ℃时18 mL水。它们所含分子数最多的是,所含原子数最多的是,质量最大的是,所含电子数最多的是(填序号)
个氮气分子④4 ℃时18 mL水。它们所含分子数最多的是,所含原子数最多的是,质量最大的是,所含电子数最多的是(填序号)
经实验测定,在4 ℃时,水的密度最大,为1 g·mL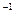 ,请计算一下,4 ℃时1 L水中含有的水分子数为,每个水分子的质量为。
,请计算一下,4 ℃时1 L水中含有的水分子数为,每个水分子的质量为。