足量铜与一定量浓硝酸反应得到硝酸铜溶液和、、 的混合气体,这些气体与1.68L(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol/L溶液至恰好完全沉淀,则消耗溶液的体积是()
| A. | 60mL | B. | 45mL | C. | 30mL | D. | 15mL |
图装置中发生反应的离子方程式为:Zn+2H+→Zn2++H2↑,下列说法错误的是
| A.a、b不可能是同种材料的电极 |
| B.该装置可能是电解池,电解质溶液为稀盐酸 |
| C.该装置可能是原电池,电解质溶液为稀盐酸 |
| D.该装置可看作是铜-锌原电池,电解质溶液是稀硫酸 |
下列电解质溶液的有关叙述正确的是
| A.在含有AgCl沉淀的溶液中加入NaCl固体,c(Ag+)增大 |
| B.在NH4Cl溶液中加入适量盐酸,可使c(NH4+)=c(Cl-) |
C.含l mol KOH的溶液与l mol CO2完全反应后,溶液中c(K+)>c(HCO )>c(OH-)>c(H+)>c(CO32-) )>c(OH-)>c(H+)>c(CO32-) |
| D.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7 |
有机物的种类繁多,但其命名是有规则的。下列有机物命名正确的是
有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成:①CH3COONa与HCl;②CH3COONa与NaOH③CH3COONa与NaCl④CH3COONa与NaHCO3
下列各项排序正确的是
| A.pH:②>③>④>① | B.c(CH3COO-):②>④>③>① |
| C.溶液中c(H+):①>③>②>④ | D.c(CH3COOH):①>④>③>② |
将右图所示实验装置的K闭合,下列判断正确的是
A.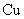 电极上发生还原反应 电极上发生还原反应 |
B.电子沿Zn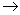 a a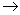 b b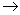 Cu路径流动 Cu路径流动 |
| C.片刻后甲池中c(SO42—)增大 |
| D.片刻后可观察到滤纸b点变红色 |