下列陈述I、II均正确且有因果关系的是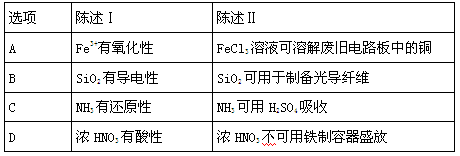
利用实验器材(规格和数量不限),能完成相应实验的一项是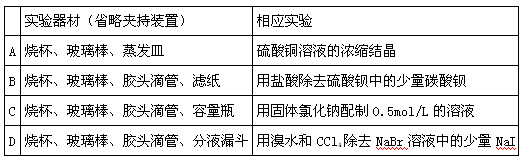
X、Y、Z为同一短周期中的元素,其原子半径依次减小,它们的最高价氧化物对应的水化物之间,任意两种混合均可反应,M为Y、Z形成的化合物,其溶液显酸性。下列说法正确的是
| A.X、Y、Z简单离子的半径依次增大 |
| B.将M溶液加热蒸干并灼烧,最后可得Y的氧化物 |
| C.Y的最高价氧化物为碱性氧化物 |
| D.将少量X单质投入到M溶液中,会置换出Y单质 |
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.标准状况下,11.2 L CCl4中含有的C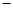 Cl键的个数为2NA Cl键的个数为2NA |
| B.1 mol Na2O和Na2O2中含有的阴、阳离子总数是3 NA |
| C.常温下,0.1 mol Cl2通入NaOH溶液中充分反应,转移电子数为0.2 NA |
| D.1 L 0.1 mol·L-1氨水溶液中所含的离子和分子总数大于0.1 NA但小于0.2 NA |
下列叙述错误的是
| A.铝热反应中可得到铁,但工业上不用该反应来大量生产铁 |
| B.可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 |
| C.明矾和漂白粉常用于自来水的净化和杀菌消毒,两者原理相同 |
| D.生成盐和水的反应不一定是中和反应 |