为达到预期的实验目的,下列操作正确的是
| A.配制0.1mol/L的盐酸500mL,应选用的仪器有胶头滴管、烧杯、玻璃棒、天平、500mL容量瓶 |
| B.欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 |
| C.为鉴别KCl、AlCl3和MgCl2溶液,分别向三种溶液中滴加NaOH溶液至过量 |
| D.测定硫酸铜晶体中结晶水含量, 加热坩埚中晶体完全失水后需在空气中冷却,再称量 |
常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,甲充有二氧化氮(N2O4 2NO2△H> 0)乙充有空气,现分别进行下列两个实验:
2NO2△H> 0)乙充有空气,现分别进行下列两个实验:
(a)将两容器置于沸水中加热(b)在活塞上都加2 kg的砝码
在以上两情况下,甲和乙容器的体积大小的比较,正确的是
A.(a)甲>乙,(b)甲>乙 B.(a)甲>乙,(b)甲<乙
C .(a)甲<乙,(b)甲>乙 D.(a)甲>乙,(b)甲=乙
.(a)甲<乙,(b)甲>乙 D.(a)甲>乙,(b)甲=乙
一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20.0%,与反应前的体积相比,反应后体积缩小的百分率是
| A.80.0% | B.20.0% | C.16.7% | D.83.3% |
已知化学反应的热效应只与反应物的初始状态和生成物的最终状态有关,如图(Ⅰ)所示:ΔH1=ΔH2+ΔH3;根据上述原理和图(Ⅱ)所示,判断各对应的反应热关系中不正确的是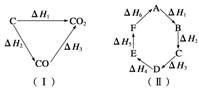
| A.A―→F ΔH=-ΔH6 |
| B.A―→D ΔH=ΔH1+ΔH2+ΔH3 |
| C.ΔH1+ΔH2+ΔH3+ΔH4+ΔH5+ΔH6=0 |
| D.ΔH1+ΔH6=ΔH2+ΔH3+ΔH4+ΔH5 |
在密闭容器中充入4molX,在一定温度下4X(g)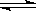 3Y(g)+Z(g)达到平衡时,有30%的X发生分解,则平衡时混合气体总的物质的量是
3Y(g)+Z(g)达到平衡时,有30%的X发生分解,则平衡时混合气体总的物质的量是
| A.4mol | B.3.4mol | C.2.8mol | D.1.2mol |
合成氨反应:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1,在反应过程中,正反应速率的变化如下图。下列说法正确的是
2NH3(g) ΔH=-92.4 kJ·mol-1,在反应过程中,正反应速率的变化如下图。下列说法正确的是
| A.t1时升高了温度 | B.t2时使用了催化剂 |
| C.t3时增大了压强 | D.t4时降低了温度 |