工业上冶炼钼的化学原理为
①2MoS2+7O2 2MoO3+4SO2
2MoO3+4SO2
②MoO3+2NH3·H2O====(NH4)2MoO4+H2O
③(NH4)2MoO4+2HCl====H2MoO4↓+2NH4Cl
④H2MoO4 MoO3+H2O
MoO3+H2O
⑤用还原剂将MoO3还原成金属钼。下列说法正确的是 ( )
| A.MoS2高温煅烧反应中MoS2既是氧化剂又是还原剂 |
| B.MoO3是金属氧化物,属于碱性氧化物 |
| C.H2MoO4是一种强酸 |
| D.利用H2、CO和铝分别还原等物质的量的MoO3 得到Mo,所消耗三种还原剂的物质的量之比为3:3:2 |
W、X、Y、Z是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Y元素形成的单质,常温下丙和己均为气体。已知反应:甲+乙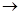 丁+己,甲+丙
丁+己,甲+丙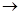 戊+己;常温下0.01 mol·L-1丁溶液的pH为12。下列说法正确的是
戊+己;常温下0.01 mol·L-1丁溶液的pH为12。下列说法正确的是
| A.元素X在周期表中的位置为第2周期ⅥA族 |
| B.元素X、Y、Z的原子半径由大到小的顺序为r(Z)>r(Y)>r(X) |
| C.1 mol甲与足量的乙完全反应转移的电子数为6.02×1023 |
| D.1.0 L0.1 mol·L-1戊溶液中阴离子的总物质的量小于0.1 mol |
如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是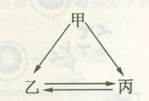
①C;②H2O2;③Na;④Fe;⑤HNO3
| A.仅①③④ | B.仅①②⑤ |
| C.仅①②③⑤ | D.①②③④⑤ |
化学与生产生活、环境保护密切相关。下列说法中不正确的是
| A.加热能杀死流感病毒是因为病毒的蛋白质受热变性 |
| B.人造纤维、合成纤维和光导纤维都是有机高分子化合物 |
| C.方便面的制作过程中常用到纯碱,葡萄酒中一般加入少量SO2作为添加剂 |
| D.绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染 |
下列说法正确的是
| A.pH=5的NH4 Cl溶液或醋酸中,由水电离出的c(H+)均为10-9 mol/L |
| B.常温时将pH=3的醋酸和pH=ll的NaOH溶液等体积混合后,pH >7 |
| C.在c(H+):c(OH-)=1:l012的溶液中,N a+、I-、NO3-、SO42-能大量共存 |
| D.0.1 mol/L Na2 CO3溶液和0.1 mol/L NaHSO4溶液等体积混合,溶液中 |
c(Na+)+c( H+) =c(CO32-)+c( SO42-)+C( HCO3-)+c(OH-)
下列说法正确的是
A.检验某酸性溶液中C1-和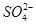 ,选用试剂及顺序是过量Ba(NO3)2溶液、AgNO3溶液 ,选用试剂及顺序是过量Ba(NO3)2溶液、AgNO3溶液 |
| B.将CO2和SO2混合气体分别通人BaC12溶液、Ba(NO3)2溶液中,最终都有沉淀生成 |
| C.将铁粉加入FeCl3、CuCl2混合溶液中,充分反应后剩余的固体中必有铁 |
| D.用加热分解的方法可将NH4Cl固体和Ca(OH)2固体的混合物分离 |