已知:G 是一种常用的药用有机物,合成路线如图所示: 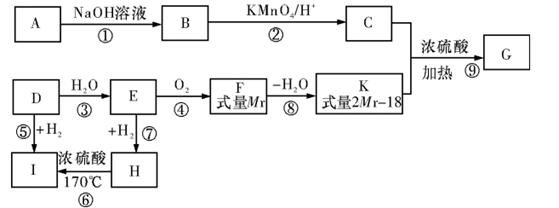
①有机物A 和C都能与FeCl3发生显色反应,且每个分子中两个取代基处于邻位,5.4gA
与标准状况下9.52LO2刚好完全燃烧生成15.4gCO2 和3.6gH2O;
②有机物G只含碳、氢、氧元素且式量小于200,氧元素的质量分数为35.56%。请回
答:
(1)写出A、C的结构简式A ,C 。
(2)反应②~⑨中,属于取代反应的有 (填序号)。
(3)写出F的常见同分异构体与F在浓硫酸作用下反应的化学方程式
。
(4)写出G在加热条件下与NaOH溶液反应的化学方程式
。
(5)写出反应⑥的方程式 。
有第四周期的A、B、C、D四种元素,其价电子数依次为1、2、2、7,其原子序数依A、B、C、D依次增大。已知A与B的次外层电子数为8,而C与D为18。根据原子结构,判断:
(1)哪些是金属元素?__________。
(2)D与A的简单离子是 __________。
(3)__________元素的氢氧化物碱性最强。
(4)B与D的两原子间能形成的化合物是____________________(写出化学式)。
有机物
是最常用的食用油氧化剂,分子式为
,可发生如下转化:



 已知
的相对分子质量为60,分子中只含一个甲基。
的结构可表示为:
已知
的相对分子质量为60,分子中只含一个甲基。
的结构可表示为:

 请回答下列问题:
请回答下列问题: (1)根据系统命名法,
的名称为。
(1)根据系统命名法,
的名称为。 (2)官能团
的名称为,高聚物
的链节为。
(2)官能团
的名称为,高聚物
的链节为。 (3)
的结构简式为。
(3)
的结构简式为。 (4)反应⑤的化学方程式为。
(4)反应⑤的化学方程式为。 (5)
有多种同分异构体,写出期中2种符合下列要求的同分异构体的结构简式。
(5)
有多种同分异构体,写出期中2种符合下列要求的同分异构体的结构简式。 i.含有苯环 ii.能发生银镜反应 iii.不能发生水解反应
i.含有苯环 ii.能发生银镜反应 iii.不能发生水解反应 (6)从分子结构上看,
具有抗氧化作用的主要原因是(填序号)。
(6)从分子结构上看,
具有抗氧化作用的主要原因是(填序号)。 a.含有苯环 b.含有羰基c.含有酚羟基
a.含有苯环 b.含有羰基c.含有酚羟基
写出下列反应的化学方程式,是离子反应的写离子方程式。
(1)少量SO2气体通入到NaOH溶液中:____________。
(2)过量SO2气体通入到澄清石灰水中:___________。
(3)SO2气体通入到碘水中:_____________________。
(4)H2S气体与SO2气体混合:___________________。
(5)SO2和O2的反应:__________________________。
(6)SO2气体通入到少量Na2CO3溶液中____________
已知盐酸加到品红溶液中,使品红溶液的红色加深。试推测:
(1)向品红溶液中通过量SO2的过程中的现象为__________;加热后的现象为___________。
(2)向品红溶液中通入过量Cl2的过程中,观察到的现象为___________。
(3)向品红溶液中通入物质的量比为1∶1且足量的SO2和Cl2后现象为______________。
亚硫酸钠中有+4价的硫,它既有氧化性又有还原性。现有试剂:溴水、硫化钠溶液、Na2SO4、稀H2SO4、NaOH溶液、氨水。
(1)要证明Na2SO3具有还原性,应选用的试剂有________;看到的现象是________;反应的离子方程式为_______________。
(2)要证明Na2SO3具有氧化性________,应选用的试剂有_________;看到的现象是_______;反应的离子方程式为_______________。