已知A的产量通常用来衡量一个国家的石油化工水平,D的结构可用右下图模型表示。现以A为主要原料合成F和高分子化合物E,其合成路线如下图所示。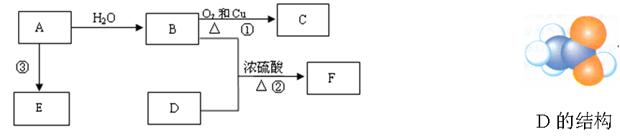
(1)A的结构式为 。 B中含官能团名称为 ;
;
(2)写出反应的化学方程式
①: 反应类型:
②: 反应类型:
(3)实验室怎样鉴别B和D?
(4)在实验室里我们可以用如图所示的装置来制取F,乙中所盛的试剂为 ,该溶液的主要作用是 ;该装置图中有一个明显的错误是 。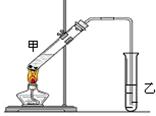
钛白粉(主要成分是Ti02),覆盖能力强,折射率高,无毒,广泛用于油漆、塑料、造纸等行业,还可用作乙醇脱水、脱氢的催化剂。下图是以钛铁矿(主要成分FeTi03,钛酸亚铁)为主要原料生产钛白粉的工艺流程图,回答下列问题:
(1)上述生产流程中加入物质A的目的是防止Fe2+被氧化,物质A是;上述制备Ti02的过程中,所得到的副产物是,可回收利用的物质是:___________________。
(2)写出TiOS04溶液在加热条件下水解反应的离子方程式:
(3)为测定TiOS04的含量,首先取待测钛液10 mL用水稀释至100 mL,加过量铝粉,充分振荡,使其完全反应:3Ti02+ +Al+6H+==3Ti3++AL3++3H20。过滤后,取出滤液20 mL,向其中滴加2~3滴KSCN溶液作指示剂,用酸式滴定管滴加0.1mol·L-1 FeCl3溶液,当溶液出现红色达到滴定终点,用去了30mL FeC13溶液。待测钛液中TiOS04的物质的量浓度是____________________。
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中C02的含量及有效地开发利用CO2,引起了各国的普遍重视。
(1)下列关于C02的用途不正确的是(填序号)。
| A.二氧化碳能溶于水,可用于生产碳酸型饮料 |
| B.固体二氧化碳俗称干冰,可用于人工降雨 |
| C.二氧化碳用于灭火是因为降低了可燃物的着火点 |
| D.超临界二氧化碳作萃取溶剂用于从天然产物提取和净化活性组分 |
E.二氧化碳可以作为气肥,提高农作物的产量
(2)目前工业上有一种方法是用C02来生产甲醇。为探究其反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0kJ.m01-1,测得C02和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0kJ.m01-1,测得C02和CH3OH(g)的浓度随时间变化如图所示。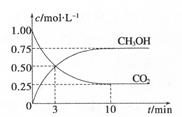
①从反应开始到平衡,氢气的平均反应速率:v(H。)=。
②该反应的平衡常数为。
(3)以KHC03溶液为电解质,用电解的方法也可以将CO2还原为甲醇。请写出电解时阴极的离子方程式:
(4)金刚石、石墨烯、线型碳是碳的几种同素异形体。从键的类型分析它们的稳定性由强到弱的顺序为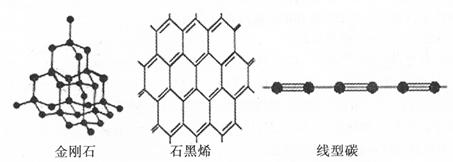
前四周期元素X、Y、Z、M、N原子序数依次增大,其中有两种是金属元素,X单质是密度最小的物质,Y原子最外层电子数是次外层的两倍,Z单质是大气中的一种气体,豆科植物常温下能将之转化为化合物。M元素的p电子总数比s电子总数多1,N是一种生命元素,人体缺少该元素会发生贫血,使人脸色萎黄。
请根据上述信息,回答下列问题:
(1)写出M原子基态电子排布式。
(2)直线型分子Y2Z2中所有原子都达到8电子稳定结构,其中δ键、 键之比是。
键之比是。
(3)上述五种元素能形成的晶体类型有(填编号)。
①原子晶体②分子晶体③离子晶体④金属晶体
(4)已知:298 K时固体M在氧气中燃烧生成1 mol M203固体时,放出热量1676.2 kJ;固
体N在氧气中燃烧生成1 mol N304固体时,放出热量1118.4 kJ。请写出298 K时,由M
单质与Z304反应的热化学方程式:
(5)在沸水中加入N的某高价盐饱和溶液可以得到一种红褐色的液体,向该液体中逐滴加入含Z的最高价氧化物的水化物溶液直至过量的过程中发生的现象是____。
砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%,推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措,已知砷化镓的晶胞结构如图。试回答下列问题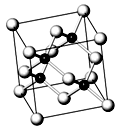
(1)下列说法正确的是(选填序号)。
A.砷化镓晶胞结构与NaCl相同 B.第一电离能:As>Ga
C.电负性:As>Ga D.砷和镓都属于p区元素
E.半导体GaP、SiC与砷化镓为等电子体
(2)砷化镓是将(CH3)3Ga和AsH3用MOCVD方法制备得到,该反应在700℃进行,反应的方程式为:。
AsH3空间形状为:(CH3)3Ga中镓原子杂化方式为:。
(3)Ga的核外价电子排布式为:。
(4)AsH3沸点比NH3低,其原因是:。
在一个装有可移动活塞的容器中模拟传统工业合成氨的反应:N2(g)+3H2(g)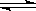 2NH3(g),反应达到平衡后,测得NH3的物质的量为amol
2NH3(g),反应达到平衡后,测得NH3的物质的量为amol
(1)保持容器内的温度和压强不变,向平衡体系中又通入少量的H2,再次达到平衡后,测得NH3的物质的量为bmol,则 ab(填入“>”或“<”或“=”或“无法确定”,下同)。若向平衡体系中通入的是少量N2,则 ab。
煤制油是一项新兴的、科技含量较高的煤化工技术,发展煤制油对我国而言具有重大意义。下列是煤通过间接液化技术制汽油和丙烯的主要工艺流程图。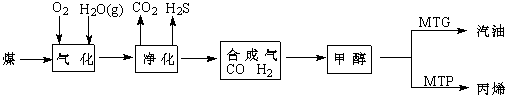
已知甲醇制烃的反应原理为: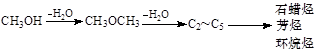
(2)为了提高原料利用率,上述工艺中应控制合成气中V(CO):V(H2)=。
(3)由二甲醚在催化剂作用下转化为丙烯的化学方程式为:。
(4)每生产1t甲醇约耗煤1.5t,每生产1 t汽油约需耗2.4t甲醇,2015年我国煤制油将达到1000万吨,则2015年当年需消耗原煤约万吨。
(5)采用MTG法生产的汽油中,均四甲苯(1,2,4,5-四甲基苯)质量分数约占4 %~7%,均四甲苯的结构简式为:。
(6)采用DMTO技术,若获得乙烯和丙烯及丁烯3种烃,生成丁烯的选择性(转化丁烯的甲醇的物质的量与甲醇总物质的量之比)为20%,其余生成乙烯和丙烯,设丙烯的选择性为x,今有403.2L(标准状况)合成气,且完全转化为甲醇,甲醇转化为烯烃的总转化率亦为100%,请作出丙烯的物质的量随x变化的曲线。