有一混合溶液,其中只含有Fe2+、Cl-、Br-、I-(忽略水的电离),其中Cl-、Br-、I-的个数比为2∶3∶4,向该溶液中通入氯气,使溶液中Cl-和Br-的个数比为3∶1,则通入氯气的物质的量与溶液中剩余的Fe2+的物质的量之比为
(已知:还原性I->Fe2+>Br->Cl-)
| A.7∶1 | B.7∶2 | C.7∶3 | D.7∶4 |
如下图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是( )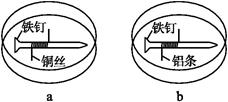
| A.a中铁钉附近呈现红色 | B.b中铁钉上发生还原反应 |
| C.a中铜丝上发生氧化反应 | D.b中铝条附近有气泡产生 |
按下图装置实验,若x轴表示流出负极的电子的物质的量,则y轴应表示( )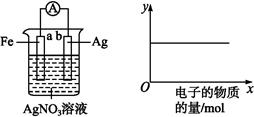
①c(Ag+) ②c(N) ③a棒的质量 ④b棒的质量
⑤溶液的质量
| A.①③ | B.③④ | C.①②④ | D.② |
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池。①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少,据此判断这四种金属活动性由大到小的顺序是( )
| A.①③②④ | B.①③④② |
| C.③④②① | D.③①②④ |
如图所示,X为单质硅,Y为金属铁,a为NaOH溶液,组装成一个原电池,下列说法中正确的是( )
A.X为负极,电极反应为:Si-4e- Si4+ Si4+ |
B.X为正极,电极反应为:4H2O+4e- 4OH-+2H2↑ 4OH-+2H2↑ |
C.X为负极,电极反应为:Si+6OH--4e- Si+3H2O Si+3H2O |
D.Y为负极,电极反应为:Fe-2e- Fe2+ Fe2+ |
下图是锌、铜和稀硫酸形成的原电池,某实验兴趣小组同学做完实验后,在读书卡片上记录如下:

卡片上的描述合理的是( )
| A.①②③ | B.③④⑤ | C.①⑤⑥ | D.②③④ |