有机物的结构简式如下图,则此有机物可发生的反应类型有: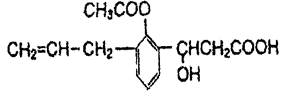
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和
| A.①②③⑤⑥ |
| B.②③④⑤⑥ |
| C.①②③④⑤⑥⑦ |
| D.②③④⑤⑥⑦ |
常温下,现有0.1mol/L的NH4HCO3溶液,pH=7.8。已知含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如下图所示。下列说法不正确的是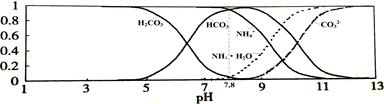
| A.NH4HCO3溶液中存在下列守恒关系:c(NH4+)+c(NH3·H2O)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| B.往该溶液中逐滴滴加氢氧化钠时NH4+和HCO3-浓度逐渐减小 |
| C.通过分析可知常温下Kb(NH3·H2O)>Ka1(H2CO3) |
| D.当溶液的pH=9时,溶液中存在下列关系:c(HCO3-)>c(NH4+)>c(NH3·H2O)>c(CO32-) |
如图是可逆反应A+2B 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
A.正反应是吸热反应
B.若A、B是气体,则D是液体或固体
C.逆反应是放热反应
D.A、B、C、D均为气体
下图甲是CO2电催化还原为碳氢化合物的工作原理示意图,用一种钾盐水溶液作电解液;图乙是用H2还原CO2制备甲醇的工作原理示意图,硫酸为电解质溶液。下列说法不正确的是

| A.甲中铜片作阴极,K+向铜片电极移动 |
B.乙中正极发生的电极反应为CO2+6e-+6H+ CH3OH+H2O CH3OH+H2O |
| C.乙中H2SO4的作用是增强溶液的导电性 |
| D.甲中若CxHy为C2H4,则生成1 mol C2H4的同时生成2 molO2 |
下列说法正确的是
| A.增大压强任何反应的反应速率都一定增大 |
B.已知H2CO3的电离常数分别为Ka1=4.3×10-7、Ka2=5.61×10-11,苯酚的电离常数Ka=1.1×10-10。苯酚钠溶液中通入少量CO2时的化学方程式为: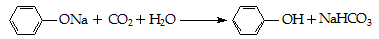 |
| C.pH=2的盐酸和pH=4的硫酸溶液等体积混合后溶液的pH=3 |
| D.在滴有酚酞的氢氧化钠溶液中逐滴滴入盐酸至红色恰好消失,此时溶液的pH=7 |
S2Cl2在合成橡胶、硬水软化等方面有着重要应用。将Cl2通入熔融的硫磺可制得S2Cl2,S2Cl2是黄红色油状发烟液体,遇水分解出无色有刺激性气味的气体,且溶液变浑浊。有关叙述正确的是
| A.在周期表中,氯元素位于硫元素之后,所以Cl2的氧化性弱于硫单质 |
| B.Cl2与硫磺的反应中,S2Cl2只是氧化产物 |
| C.在常温常压下,硫磺是原子晶体,S2Cl2是分子晶体 |
| D.S2Cl2与水反应时,既体现氧化性又体现还原性 |