下列离子方程式书写正确的是 ( )
| A.FeCl2溶液中通入Cl2: Fe2++Cl2=Fe3++2Cl- |
| B.向澄清石灰水中通入少量CO2: Ca2++2OH-+CO2=CaCO3↓+H2O |
| C.FeS固体放入稀硝酸溶液中: FeS+2H+=Fe2++H2S↑ |
| D.AlCl3溶液中加入过量烧碱溶液:Al3++4OH-=AlO2—+2H2O |
在100 mLH2SO4和CuSO4的混合液中,用石墨作电极电解一段时间,两极均收到2.24L气体(标准状况),则原混合液中,Cu2+的物质的量浓度为()
A.1mol?L―1 B.2mol?L―1 C.3 mol?L―1 D.4 mol?L―1
只用一种试剂,区别四氯化碳、己烯、碘化钾溶液、甲苯四种无色液体,应选用
| A.KMnO4酸性溶液 | B.溴水 | C.淀粉-碘化钾试剂 | D.硝酸银溶液 |
下列物质一定属于纯净物的是
| A.苯 | B.聚乙烯 | C.汽油 | D.C5H10 |
下列各组物质符合最简式相同,但既不是同系物,也不是同分异构体的是
| A.乙烯和苯 | B.1丁烯和环己烷 |
| C.丁炔和1,3丁二烯 | D.二甲苯和甲苯 |
下列各有机物的命名中正确的是
| A.CH3—CH═CH—CH3二丁烯 | B. 2—甲基—2—丙烯 2—甲基—2—丙烯 |
C.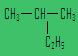 2-乙基丙烷 2-乙基丙烷 |
D. 邻氯甲苯 邻氯甲苯 |