甲烷是以碳原子为中心的正四面体结构,而不是正方形的平面结构,其理是
| A.甲烷中的四个键的键长、键角相等 | B.CH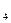 是分子晶体 是分子晶体 |
| C.二氯甲烷只有一种结构 | D.三氯甲烷只有一种结构 |
下列各组元素中既包括海水中的常量元素,又包括海水中的微量元素的是( )
A.Cl、Na、C、F B.S、Ca、U、I
C.B、F、H、Sr D.Cl、Na、Li
铜在自然界多以+1价矿石存在,因为在固态特别是高温下+1价铜的化合物比+2价稳定。从辉铜矿(Cu2S)炼铜的方法之一是:①将矿石高温通空气焙烧,生成两种氧化物。②将焙烧过的矿石加上比它质量约少一半的未经焙烧过的矿石,混合后隔绝空气再进行高温燃烧,结果得到金属铜和一种具有刺激性气味的气体。写出这两个反应的化学方程式。
已知工业上真空炼铷的反应方程式如下:2RbCl+Mg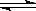 MgCl2+2Rb(g),对此反应能够进行的正确解释是( )
MgCl2+2Rb(g),对此反应能够进行的正确解释是( )
| A.铷比镁的金属性强 |
| B.铷的沸点比镁低,把铷的蒸气抽走后,平衡向正反应方向移动 |
| C.MgCl2的热稳定性比RbCl弱 |
| D.高温下Mg2+得电子能力比Rb+弱 |
金属锂是密度最小的金属,等质量的金属,锂可以释放出更多的电子,故常用来制造高性能电池。已知锂的金属性介于钠和镁之间,则冶炼金属锂应采用的方法是( )
| A.电解法 | B.热还原法 | C.热分解法 | D.铝热法 |
实验室将9 g铝粉跟一定量的金属氧化物粉末混合形成铝热剂。发生铝热反应之后,所得固体中含金属单质为18 g,则该氧化物粉末可能是( )
| A.Fe2O3和MnO2 | B.MnO2和V2O5 |
| C.Cr2O3和V2O5 | D.Fe3O4和FeO |