最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如右图所示,已知断裂1molN-N吸收167kJ热量,生成1molN≡N放出942kJ热量。根据以上信息和数据,下列说法正确的是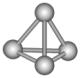
| A.N4属于一种新型的化合物 |
| B.N4与N2互为同素异形体 |
| C.N4沸点比P4(白磷)高 |
| D.1molN4气体转变为N2吸收882kJ热量 |
你认为下列实验方案中,可行的是
| A.按溶解、过滤、蒸发的操作顺序可以分离 CaCl2、CaCO3的混合物 |
| B.向某种未知溶液中加入 AgNO3溶液,产生白色沉淀,证明溶液是盐酸 |
| C.用镁在密闭容器中燃烧,除去密闭容器内空气中的氧气 |
| D.将 pH 试纸润湿后,用玻璃棒蘸取食用白醋滴在试纸上,测定其pH |
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O Cd(OH)2 +2Ni(OH)2
Cd(OH)2 +2Ni(OH)2
有关该电池的说法正确的是
| A.充电时阳极反应:Ni(OH)2-e— + OH- ="=" NiOOH + H2O |
| B.充电过程是化学能转化为电能的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH- 向正极移动 |
在25℃时,将两个铜电极插入一定量的硫酸钠饱和溶液中,进行电解,通电一段时间后,阴极逸出a mol气体,同时有wg Na2SO4•10H2O晶体析出,若温度不变,剩余溶液的溶质的质量分数为
A. ×100% ×100% |
B. ×100% ×100% |
C. % % |
D. % % |
下列与化学反应能量变化相关的叙述正确的是
| A.生成物能量低于反应物总能量时,反应吸热 |
| B.有热量变化时一定发生了化学变化 |
| C.依据盖斯定律,可计算某些难以直接测定的△H |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的△H不同 |
下列结论正确的是
①微粒半径:S2->Cl>S>F②氢化物稳定性:HF>HCl>H2S
③离子还原性:S2->Cl->Br->I- ④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>HClO4⑥非金属性:F>Cl>S
| A.②④⑥ | B.①③④ | C.只有① | D.只有⑥ |