现有下列短周期元素性质的相关数据:
| |
① |
② |
③ |
④ |
⑤ |
⑥ |
| 原子半径(10-10m) |
1.30 |
0.82 |
0.99 |
1.11 |
0.90 |
1.18 |
| 最高或最低化合价 |
+2 |
+3 |
+7 |
+4 |
+2 |
+3 |
| |
|
-1 |
-4 |
|
|
请回答下列问题:
(1)②和③形成的化合物类型为 (填“离子”或“共价”)化合物;
(2)元素①的金属性比元素⑥要 (填“强”或“弱”),试从原子结构方面解释其原因: ;
(3)在自然界中,元素④的存在形态为 ,工业上粗制该元素单质的化学方程式为 ;
(4)⑥的单质与浓NaOH溶液反应的离子方程式是 ;
(5)实验室现有元素①的单质和某未知金属单质M,请简要写出比较两者金属性强弱的一种实验方案 。
“张-烯炔环异构反应”被《Name Reactions》收录。该反应可高效构筑五元环化合物:
(R、R‘、R“表示氢、烷基或芳基)
合成五元环有机化合物J的路线如下:
已知:
(1)A属于炔烃,其结构简式是 。
(2)B由碳、氢、氧三种元素组成,相对分子质量是30。B的结构简式是
(3)C、D含有与B相同的官能团,C是芳香族化合物,E中含有的官能团是
(4)F与试剂a反应生成G的化学方程式是 ;试剂b是 。
(5)M和N均为不饱和醇。M的结构简式是 。
(6)N为顺式结构,写出N和H生成I(顺式结构)的化学方程式: 。
C、N、O、Al、Si、Cu是常见的六种元素。
(1)Si位于元素周期表第____周期第_____族。
(2)N的基态原子核外电子排布式为_____;Cu的基态原子最外层有___个电子。
(3)用“>”或“<”填空:
| 原子半径 |
电负性 |
熔点 |
沸点 |
| Al_____Si |
N____O |
金刚石_____晶体硅 |
CH4____SiH4 |
(4)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
0-t1时,原电池的负极是Al片,此时,正极的电极反应式是_____,溶液中的H+向___极移动,t1时,原电池中电子流动方向发生改变,其原因是______。
氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:
(1)反应Ⅰ的化学方程式是 。
(2)反应Ⅰ得到的产物用I2进行分离。该产物的溶液在过量I2的存在下会分成两层——含低浓度I2的H2SO4层和高浓度的I2的HI层。
①根据上述事实,下列说法正确的是 (选填序号)。
a.两层溶液的密度存在差异
b.加I2前,H2SO4溶液和HI溶液不互溶
c.I2在HI溶液中比在H2SO4溶液中易溶
②辨别两层溶液的方法是 。
③经检测,H2SO4层中c(H+):c(SO42-)=2.06:1。其比值大于2的原因是 。
(3)反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g)△H=+550kJ/mol
它由两步反应组成:i.H2SO4(l)=SO3(g) +H2O(g)△H=+177kJ/mol
ii.SO3(g)分解。
L(L1、L2),X可分别代表压强或温度。下图表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系。
①X代表的物理量是 。
②判断L1、L2的大小关系,并简述理由: 。
Ⅰ、分子式为C8H8O3的芳香族化合物有多种不同的结构,这些物质有广泛用途。
(1)C8H8O3的某一同分异构体尼泊金酯的结构简式如图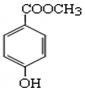
①下列对尼泊金酯的判断正确的是 。
a.能发生水解反应
b.能与FeCl3溶液发生显色反应
c.分子中所有原子都在同一平面上
d.能与浓溴水反应产生白色沉淀。
②尼泊金酯与NaOH溶液在一定条件下反应的化学方程式是 。
(2)C8H8O3的另一种同分异构体甲如图: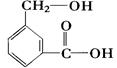
①请写出甲中所含官能团的名称 , 。
②甲在一定条件下跟Na反应的化学方程式是: 。
③甲跟NaHCO3溶液反应的化学方程式是: 。
Ⅱ、写出下列化学反应方程式:
(1)溴乙烷与NaOH的乙醇溶液共热: 。
(2)将CO2通入苯酚钠溶液中: 。
(3)1,3-丁二烯的与Br2的1、4加成反应: 。
(4)葡萄糖与银氨溶液发生银镜反应: 。
化合物H是重要的有机化合物,可由E和F在一定条件下合成:(有些反应条件省略如:加热等)
已知以下信息:
①A属于芳香烃,H属于酯类化合物。
②I的核磁共振氢谱为二组峰,且峰的面积比为6:1。
回答下列问题:
(1)B的结构简式 ,C的官能团名称 。
(2)B C;G
C;G J两步的反应类型 , 。
J两步的反应类型 , 。
(3)①E+F H的化学方程式 。
H的化学方程式 。
②I G的化学方程式 。
G的化学方程式 。
(4)H的同系物K比H相对分子质量小28,K的同分异构体中能同时满足如下条件:
①属于芳香族化合物
②能和饱和NaHCO3溶液反应放出CO2,共有______种(不考虑立体异构)。
K的一个同分异构体能发生银镜反应,也能使FeCl3溶液显紫色,苯环上有两个支链,苯环上的氢的核磁共振氢谱为二组峰,且峰面积比为1:1,写出K的这种同分异构体的结构简式 。