有两支盛硝酸钡溶液的试管,向一支里加入盐酸,向另一支里加入烧碱溶液,再同时通入SO2,都有白色沉淀生成,由此可得出的结论是
| A.两支试管里的沉淀都是亚硫酸钡 | B.SO2在两个反应中分别表现出酸性、还原性 |
| C.两支试管里的沉淀都是硫酸钡 | D.亚硫酸钡在碱性溶液里是不溶解的 |
除去CO2中SO2的气体,不能选用的试剂为( )
| A.KMnO4溶液 | B.NaHCO3溶液 | C.NaOH溶液 | D.双氧水 |
下列表示物质的图或式正确的是( )
| A.氮气的电子式N┇┇N | B.Mg2+的结构示意图 |
C.NH3的结构式 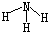 |
D.甲基的电子式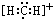 |
X元素原子的质量数为m,核内中子数为n,则Wg X2+离子含有的电子的物质的量约为( )
| A.(m+n+2)w/m mol | B. (m-n+2)w/m mol | C. (m+n-2)w/m mo l l |
D. (m-n-2)w/m mol |
A、B、C都是 金属,把A浸入C的硝酸盐溶液中,A的表面有C析出,A与B和酸溶液组成原电池时,B为电池的负极。A、B、C三种金属的活动性顺序为( )
金属,把A浸入C的硝酸盐溶液中,A的表面有C析出,A与B和酸溶液组成原电池时,B为电池的负极。A、B、C三种金属的活动性顺序为( )
A.A>B>C B.A>C>B C.B>A>C D.B>C>A
将Al片和Cu片用导线相连,一组插入浓盐酸中,一组插入稀氢氧化钠溶液中,分别形成原电池,则在这两原电池中,正极分别为( )
| A.Cu片、Cu片 | B.Cu片、Al片 | C.Al片、Al片 | D.Al片、Cu片 |