下列各溶液中,微粒的物质的量浓度关系正确的是
| A.0.1mol·L-1的(NH4)2SO4溶液中:c(SO42- )>c(NH4+ )>c(H+)>c(OH-) |
| B.0.2mol·L-1的Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| C.0.1mol·L-1的NH4Cl溶液与0.05mol· L-l的NaOH溶液等体积混合: c(Cl- ) >c(Na+ ) >c(NH4+ ) >c(OH- ) >c(H+) |
| D.c(NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4C1溶液: |
c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4C1)
人工光合作用能够借助太阳能,用CO2和H2O来制备化学原料。下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是 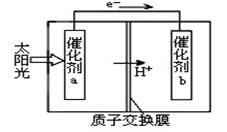
| A.该过程是将太阳能转化为化学能的过程 |
| B.催化剂a表面发生氧化反应,有O2产生 |
| C.催化剂a附近酸性减弱,催化剂b附近酸性增强 |
| D.催化剂b表面的反应是CO2 +2H++2e一=HCOOH |
关于下列各装置图的叙述中,不正确的是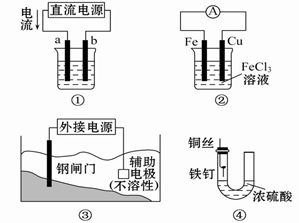
| A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 |
| B.装置②的总反应式是Cu+2Fe3+====Cu2++2Fe2+ |
| C.装置③中钢闸门应与外接电源的负极相连 |
| D.装置④中的铁钉几乎没被腐蚀 |
水热法制备Fe3O4纳米颗粒的反应为:
3Fe2++2S2O32-+O2+xOH-===Fe3O4+S4O62-+2H2O,下列说法中错误的是
| A.每生成1 mol Fe3O4,反应转移的电子总数为4 mol |
| B.Fe2+和S2O32-都是还原剂 |
C.1 mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为 mol mol |
| D.x=4 |
下图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是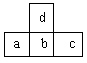
| A.a、b、c的最高价氧化物对应水化物的酸性强弱的关系是c>b>a |
| B.d的氢化物比b的氢化物稳定 |
| C.d与c不能形成化合物 |
| D.原子半径的大小顺序是a>b>c>d |
用NA表示阿伏加德罗常数的值。下列叙述中正确的是
| A.常温常压下1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
| B.1.0 L 1.0 mol·L-1的NaAlO2水溶液中含有的氧原子数为2NA |
| C.18 g D2O含有NA个质子 |
| D.0.5 mol·L-1硫酸钾溶液中阴离子所带电荷数为NA |