以A和乙醇为基础原料合成香料甲的流程图如下:

杏仁中含有A,A能发生银镜反应。质谱测定,A的相对分子质量为106。5.3g A完全燃烧时,生成15.4g CO2和2.7g H2O。
(1)A的分子式 ,A发生银镜反应的化学方程式为 。
(2)写出反应②的化学方程式 。
(3)上述反应中属于取代反应的是 。
(4)写出符合下列条件E的同分异构体有 种;
a.能发生银镜反应 b.不含-CH3 c.不能水解
写出其中能使FeCl3溶液显紫色,且苯环上的一溴代物有四种的同分异构体的结构简式 。
(5)写出反应⑤的化学方程式 。
以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
回答下列问题:
(1)在一定条件下,SO2转化为SO3的反应为2SO2(g)+O2(g)2SO3(g),该反应的平衡常数表达式为K=________;过量的SO2与NaOH溶液反应的化学方程式为
_____________________________________________________________。
(2)酸溶及后续过程中均需保持盐酸过量,其目的是________、________。
(3)通氯气氧化时,发生的主要反应的离子方程式为____________;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为________(写化学式)。
铝是地壳中含量最多的金属元素,1854年法国化学家德维尔用金属钠还原氯化钠和氯化铝的复盐,获得了铝单质。1886年,美国人豪尔和法国人海郎特,分别独立地电解熔融的氧化铝和冰晶石的混合物,制得了金属铝,奠定了今天大规模生产铝的基础。
工业生产金属铝的原料是铝土矿(主要成分为Al2O3,另含有Fe2O3和SiO2),工业中得到较纯氧化铝的过程如下图所示:
试回答下列问题:
(1)操作Ⅰ是一种重要的混合物分离方法,实验室进行该项操作用到的玻璃仪器有烧杯、________、________。
(2)经分析不溶物A的主要成分为________。
(3)工业上电解冶炼铝的化学方程式为________________,若电路中通过1 mol电子,可以得到铝________g。
(4)为了提高综合经济效益,实际工业生产中常将上述反应中的相关物质循环利用。其部分转化关系如下图所示: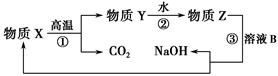
①上述转化中未涉及四种基本反应类型中的________反应;
②写出过程③的化学方程式:____________。
(5)科学研究表明,人体过量吸入铝元素会严重危害身体健康。请你结合实际提出两条杜绝铝元素过量吸入的措施:____________。
钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域。V2O5是接触法制硫酸的催化剂。
(1)一定条件下,SO2与空气反应t min后,SO2和SO3物质的量浓度分别为a mol·L-1和b mol·L-1,则SO2起始物质的量浓度为________ mol·L-1;生成SO3的化学反应速率为________ mol·L-1·min-1。
(2)工业制硫酸,尾气SO2用________吸收。
下面是一种燃煤烟气脱硫方法的原理:用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4。
其中氨水吸收燃煤烟气中SO2的化学反应为:
2NH3+SO2+H2O=(NH4)2SO3;(NH4)2SO3+SO2+H2O=2NH4HSO3
能提高燃煤烟气中SO2去除率的措施有________(填字母)。
①增大氨水浓度
②升高反应温度
③使燃煤烟气与氨水充分接触
④通入空气使HSO3-转化为SO42-
| A.①② | B.①②③④ | C.①③ | D.②③④ |
读某城市的城市布局示意图,回答有关问题:
①煤炭基地 ②大型硫酸厂 ③自来水厂 ④疗养院 ⑤大型商场 ⑥食品厂 ⑦化工厂 ⑧造纸厂 ⑨污水处理厂 ⑩高等院校
(1)该城市布局是否合理?请分析原因。
(2)图中②处分布大型硫铁矿(主要成分是FeS2)。写出制取二氧化硫、三氧化硫的化学方程式。
(3)接触法制硫酸的尾气中还含有少量的二氧化硫,如果排入大气,就会造成环境污染。你认为该企业应该采用什么方法回收、利用尾气中的二氧化硫,写出有关反应的化学方程式。
(4)该市经济发达,每天有大量的汽车排放氮氧化合物、碳氢化合物,以及企业、家庭炉灶排放大量的二氧化硫、二氧化碳等,该市应采取哪些措施防治大气污染?