银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为:
2Ag+Zn(OH)2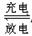 Ag2O+Zn+H2O在此电池放电时,负极上发生反应的物质是
Ag2O+Zn+H2O在此电池放电时,负极上发生反应的物质是
| A.Ag | B.Zn(OH)2 | C.Ag2O | D.Zn |
原子序数为83的元素位于:①第5周期;②第6周期;③ⅣA族;④ⅤA族;⑤ⅡB族,其中正确的组合是()。
| A.①④ | B.②③ | C.②④ | D.①⑤ |
关于同一种元素的原子或离子,下列叙述正确的是()。
| A.原子半径比阴离子半径小 |
| B.原子半径比阴离子半径大 |
| C.原子半径比阳离子半径小 |
| D.带正电荷多的阳离子比带正电荷少的阳离子半径大 |
下列微粒半径大小比较错误的是()。
| A.K>Na>Li | B.Na+>Mg2+>Al3+ |
| C.Mg2+>Na+>F- | D.Cl->F->F |
下列关于微粒半径的叙述中,正确的是()。
| A.金属阳离子的半径大于它的原子半径 |
| B.金属阳离子的半径小于它的原子半径 |
| C.非金属阴离子的半径与其原子半径相等 |
| D.非金属阴离子的半径小于其原子半径 |
元素的原子半径在周期表中呈现周期性变化的根本原因是()。
| A.原子的相对原子质量呈现周期性变化 |
| B.元素的化合价呈现周期性变化 |
| C.原子的性质呈现周期性变化 |
| D.元素原子的核外电子排布呈周期性变化 |