lmol某烃CmHn在氧气中完全燃烧生成水和CO2,则消耗的氧气的物质的量为
| A.2m+n/2 | B.2m+n | C.m+n/4 | D.m+n/2 |
将13.0g Al、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生气体6.72L(标况)。另取等质量的合金溶于过量的稀硝酸中生成6.72L(标况)NO,向反应后的溶液中加入过量的NaOH溶液,得到沉淀的质量是
| A.11.85g | B.12.7g | C.27.45 g | D.28.3g |
将同温同压下的NO、NO2、O2三种气体按以下体积比混合后通入水中,气体不能完全溶于水的是
| A.1∶2∶1 | B.1∶1∶1 | C.5∶1∶4 | D.6∶2∶5 |
操作1:将1 L 1.00 mol·L-1的Na2CO3溶液逐滴加入到1 L 1.25 mol·L-1的盐酸中;操作2:将1 L 1.25 mol·L-1的盐酸逐滴加入1 L 1.00 mol·L-1的Na2CO3溶液中,两次操作产生的气体体积之比(同温同压下)是
| A.5∶2 | B.2∶5 | C.1∶1 | D.2∶1 |
金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以金红石为原料制取Ti的反应为
aTiO2 + bCl2+eC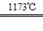 aTiCl4+eCO Ⅰ
aTiCl4+eCO Ⅰ
TiCl4+2Mg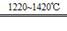 Ti+2MgCl2Ⅱ
Ti+2MgCl2Ⅱ
关于反应Ⅰ、Ⅱ的分析不正确的是
①TiCl4在反应Ⅰ中是还原产物,在反应Ⅱ中是氧化剂;②C、Mg在两个反应中均被还原;
③在反应Ⅰ、Ⅱ中Mg的还原性大于C,C的还原性大于TiCl4;
④a=1,b="e" =2 ⑤每生成19.2 g Ti,反应Ⅰ、Ⅱ中共转移4.8 mol e-。
A.①②④B.②③④C.③④D.②③⑤
已知:还原性HSO3¯>I¯,氧化性IO3¯> I2。在含3 mol NaHSO3的溶液中逐滴加入KIO3
溶液。加入KIO3和析出I2的物质的量的关系曲线如下图所示。下列说法不正确的是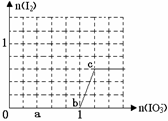
| A.0~b间反应:3HSO3-+ IO3-= 3SO42-+ I-+ 3H+ |
| B.a点时消耗NaHSO3的物质的量为1.2 mol |
| C.b~c间反应:I2仅是氧化产物 |
| D.当溶液中I¯与I2的物质的量之比为5∶2时,加入的KIO3 为1.08mol |