下列物质中既能与氢氧化钠溶液反应,又能与稀硫酸溶液反应的是( )
①Al ②Al(OH)3 ③Al2O3 ④NaHCO 3 ⑤苯 ⑥乙炔 ⑦醋酸
3 ⑤苯 ⑥乙炔 ⑦醋酸
⑧乙酸乙酯 ⑨蛋白质
| A.①②③⑦⑧⑨ | B.①②③④⑧⑨ | C.②④③⑥⑦⑧⑨ | D.全部 |
在常温常压时,充分燃烧一定量的丁烷(C4H10)气体,放出热量Q kJ(Q>0),将生成的二氧化碳全部通入足量NaOH溶液中,发生的反应为:CO2 + 2NaOH = Na2CO3 + H2O,共消耗了4mol·L-1的NaOH溶液200 mL。则此条件下,下列热化学方程式正确的是 ( )
A.C4H10(g)+ O2(g)===4CO2(g)+5H2O(l) ΔH=-Q kJ·mol-1 O2(g)===4CO2(g)+5H2O(l) ΔH=-Q kJ·mol-1 |
B.C4H10(g)+ O2(g)===4CO2(g)+5H2O(l)ΔH=-10Q kJ·mol-1 O2(g)===4CO2(g)+5H2O(l)ΔH=-10Q kJ·mol-1 |
C.C4H10(g)+ O2(g)===4CO2(g)+5H2O(l)ΔH=+ 10Q kJ·mol-1 O2(g)===4CO2(g)+5H2O(l)ΔH=+ 10Q kJ·mol-1 |
D.C4H10(g)+ O2(g)===4CO2(g)+5H2O(g)ΔH=-10Q kJ O2(g)===4CO2(g)+5H2O(g)ΔH=-10Q kJ |
右图为直流电源电解稀Na2SO4溶液的装置。通电一段时间后,在石墨电极a和b附近分别滴加一滴酚酞溶液。则下列有关说法中正确的是( )
| A.a电极产生H2 |
| B.两极产生的气体均有刺激性气味 |
| C.通电一段时间后,稀Na2SO4溶液酸性增强 |
| D.a电极附近呈无色,b电极附近呈红色 |
碘与氢气反应的热化学方程式是
①I2(g)+H2(g) 2HI(g)ΔH=-9.48 kJ·mol-1②I2(s)+H2(g)
2HI(g)ΔH=-9.48 kJ·mol-1②I2(s)+H2(g) 2HI(g)ΔH="+26.48" kJ·mol-1下列说法正确的是( )
2HI(g)ΔH="+26.48" kJ·mol-1下列说法正确的是( )
| A.从上述两反应可知1mol的I2(g)能量比1mol的I2(s)能量高 |
B.I2(s) I2(g) ΔH<0 I2(g) ΔH<0 |
| C.②的反应物总能量与①的反应物总能量相等 |
| D.1 mol I2(g)中通入1 mol H2(g),发生反应时放出的热量为9.48 kJ·mol-1 |
下图有关电化学的示意图正确的是()
如图由锌—铜—稀H2SO4组成的原电池装置中,当导线中有0.2 mol电子通过时,理论上两极的变化是()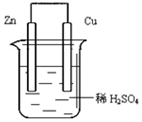
| A.铜片增重6.4g | B.锌片增重6.5 g |
| C.铜片上析出0.1 mol O2 | D.锌片溶解了6.5 g |