探究有关物质氧化性的强弱。Bi位于元素周期表中第VA族,+3价较稳定,NaBiO3溶液为无色。取一定量的Mn(NO3)2溶液依次进行实验,现象记录如下:①滴加适量的NaBiO3溶液,溶液变为紫红色;②继续滴加适量H2O2, 紫红色褪去,并有气泡产生;③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色;④最后通入足量的SO2气体。请回答下列问题:
(1)推测实验④中现象为 。
(2)分析上述现象,KMnO4、H2O2、PbO2的氧化性由强到弱的顺序是 。
(3)写出②的离子方程式 。
(4)写出④的离子方程式 。
用于金属焊接的某种焊条,其药皮由大理石、水泥、硅铁等配制而成。
(1)Al的原子结构示意图为_________;Al与NaOH溶液反应的离子方程式为_____________.
(2) 的原子的中子数为_________;
的原子的中子数为_________;
(3)Al3+与Yn-的电子数相同,Y所在族的各元素的氢化物的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是________。
(4)焊接过程中,药皮在高温下产生了熔渣和使金属不被氧化的气体,该气体是__________。
(5)经处理后的熔渣36.0g(仅含Fe2O3、Al2O3、SiO2),加入足量稀盐酸,分离得到11.0g固体;滤液中加入过量NaOH溶液,分离得到21.4g固体;则此熔渣中Al2O3的质量分数为__________________。
下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。
已知:
①反应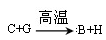 能放出大量的热,该反应曾应用于铁轨的焊接;
能放出大量的热,该反应曾应用于铁轨的焊接;
②I是一种常见的温室气体,它和 可以发生反应:2E+I
可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.
2F+D,F中的E元素的质量分数为60%.
回答问题:
(1)①中反应的化学方程式为________________________________;
(2)化合物Ⅰ的电子式为______________________,它的空间构型是_________;
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量______________________;
(4)C与过量NaOH溶液反应的离子方程式为_______________________,反应后溶液与过量化合物Ⅰ反应的离子方程式为_______________________;
(5)E在I中燃烧观察到的现象是______________________。
雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为。
(2)上述反应中的氧化剂是,反应产生的气体可用吸收。
(3)As2S3和HNO3有如下反应:As2S3+ 10H++ 10NO3—=2H3AsO4+ 3S+10NO2↑+ 2H2O若生成2mol H3AsO4,则反应中转移电子的物质的量为。若将该反应设计成一原电池,则NO2应该在(填“正极”或“负极”)附近逸出。
(4)若反应产物NO2与11.2L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量(选填编号)。
a.小于0.5 mol b.等于0.5 mol c.大于0.5mol d.无法确定
肉桂酸甲酯是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精,它的分子式为C10H10O2。G为肉桂酸甲酯的一种同分异构体,其分子结构模型如图所示(图中球与球之间连线表示单键、双键等)。
以芳香烃A为原料合成G的路线如下:
①化合物E中的官能团为 __________________________(填名称)。
②E→F的反应类型是_______________________-。
③写出下列化学方程式
C→D_______________________________________________________;
E→H_______________________________________________________。
下列是中学化学中常见物质间的反应转化关系图,其中部分产物已略去,常温下,G为固体单质,B、I为液体,其余都为气体.A为化合物,I的浓溶液与G在加热条件下生成F、B和C。 H可用作工业上冶炼金属的还原剂。请按要求填空:
(1)写出下列物质的化学式:A:________;B:________;C:________.
(2)写出F+B→I的化学方程式_________________________________.
(3)写出G和I的浓溶液反应的化学方程式_________________________