下列实验设计及其对应的离子方程式均正确的是
| A.石灰石与硫酸反应制CO2:CaCO3 + 2H+=Ca2+ + CO2↑ + H2O |
| B.Na2O2与H2O反应制备O2:Na2O2 + H2O= 2Na+ + 2OH- + O2↑ |
| C.将氯气溶于水制备次氯酸:Cl2 + H2O= 2H+ + Cl- + ClO- |
| D.用硫酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性: |
2MnO + 6H+ + 5H2O2= 2Mn2+ + 5O2↑ + 8H2O
+ 6H+ + 5H2O2= 2Mn2+ + 5O2↑ + 8H2O
下列离子方程式书写正确的是()
| A.盐酸滴人氨水中:H++OH-一H2O |
B.过量的SO2通人NaOH溶液中:SO2+20H-=SO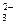 十H2O 十H2O |
| C.Fe(NO2)2溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++2H2O |
| D.硫酸亚铁溶液与稀硫酸、双氧水混合:2Fe2++H2O2+2H+=2Fe3++2H2O |
金刚烷的结构如右图,它可看作是由四个等同的六元环组成的空间构型。请根据中学学过的异构现象判断由氯原子取代金刚烷亚甲基(一CH2一)中氢原子所形成的二氯取代物的种类()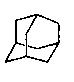
| A.2种 | B.3种 | C.4种 | D.6种 |
下列涉及有机物的性质或应用的说法,不正确的是()
| A.苯、乙醇和乙酸都能发生取代反应 |
| B.用新制的Cu(OH)2可检验尿液中的葡萄糖 |
| C.甲烷和氯气的混合气体在光照下反应生成的是一氯甲烷和氯化氢 |
| D.油脂在碱的催化作用下可发生水解,工业上利用该反应生产肥皂 |
下列有关比较中,大小顺序排列不正确的是()
| A.物质的熔点:石英>食盐>冰 |
| B.热稳定性:PH3>H2 S>HBr>NH3 |
C.结合H’的能力:CO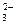 >CH3COO >SO >CH3COO >SO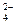 |
| D.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
在无色溶液中能大量共存的一组离子是()
| A.Na+ 、CH3COO-、CO32-、OH- | B.K+ 、Al3+、SO42-、AlO2- |
| C.Na+、K+、SO32-、Fe3+ | D.NH4+、H+、NO3-、HCO3- |