已知:①H2O(g)=H2O(l);△H=Q1 kJ·mol-1
②C2H5OH(g) = C2H 5OH(l);△H=Q2 kJ·mol-1
5OH(l);△H=Q2 kJ·mol-1
③C2H5OH(g) + 3O2(g) = 2CO2(g) + 3H2O(g);△H=Q3 kJ·mol-1
kJ·mol-1
若使23g酒精液体完全燃烧最后恢复到室温,则此反应的△H为( )
| A.Q1 + Q2 + Q3 | B.0.5(Q1 + Q2 + Q3) |
| C.0.5Q1 – 1.5Q2 + 0.5Q3 | D.1.5Q1 – 0.5Q2 + 0.5Q3 |
下列说法正确的是
| A.漂白粉的有效成分是Ca(ClO)2 |
| B.铁锈的主要成份是四氧化三铁 |
| C.NO、NO2是大气污染物,能在空气中稳定存在 |
| D.HNO3和H2SO4都是很难挥发的酸 |
下列离子方程式正确的是
| A.实验室用大理石和稀盐酸制取CO2:2H++CO32-= CO2↑+H2O |
| B.氯气与水反应:Cl2+H2O = 2H++Cl-+ClO- |
| C.氯化铝溶液加入氨水:Al3++3OH-= Al(OH)3↓ |
D.用氢氧化钠检验氯化铵溶液中铵根离子:NH4++OH―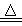 NH3 ↑+H2O NH3 ↑+H2O |
下图所示四种化学操作名称从左到右分别为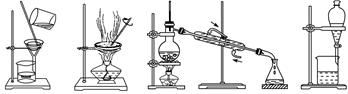
| A.过滤、蒸发、蒸馏、分液 | B.过滤、蒸馏、蒸发、分液 |
| C.蒸发、蒸馏、过滤、分液 | D.分液、蒸馏、蒸发、过滤 |
下列有关物质应用的叙述中,不正确的是
| A.少量Cl2用于饮用水消毒 | B.氧化铝用于制造耐火材料 |
| C.Na2O2用于呼吸面具中供氧 | D.Si用于制造光导纤维 |
下列物质中,既含有离子键又含有共价键的是
| A.氯化钠 | B.氢氧化钠 | C.水 | D.氯气 |