向一定量的Fe、FeO和Fe2O3的混合物中加入120mL 4mol/L的稀硝酸,恰好使混合物完全溶解,放出1.344L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为
| A.0.24mol | B.0.21mol | C.0.16mol | D.0.14mol |
在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g/cm3,溶质的质量分数为w,溶质的物质的量浓度为c mol/L。下列叙述中正确的是
①w=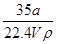 ×100% ②c=
×100% ②c=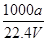
③向上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5 w
④向上述溶液中再加入1.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:
c(Cl-)> c(NH4+)>c(H+)>c(OH-)
| A.①③ | B.②③ | C.②④ | D.①④ |
下列说法正确的是
| A.在一定条件下,乙烯能与H2发生加成反应,苯不能与H2发生加成反应 |
| B.C2H6O和C4H10都有2种同分异构体 |
| C.乙酸乙酯、乙酸均能与NaOH反应,二者分子中官能团相同 |
| D.淀粉和蛋白质均可水解生成葡萄糖 |
组成和结构可用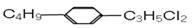 表示的有机物共有(不考虑立体异构体)
表示的有机物共有(不考虑立体异构体)
| A.9种 | B.12种 | C.24种 | D.36种 |
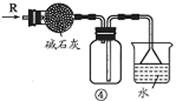
关于下列各实验装置的叙述中,不正确的是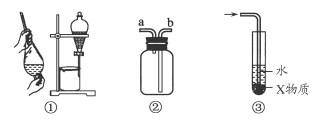
| A.装置①可用于分离C2H5OH和H2O的混合物 |
| B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 |
| C.装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 |
| D.装置④可用于干燥、收集NH3,并吸收多余的NH3 |
在一密闭容器中有CO、H2、O2共16.5g和足量的Na2O2,用电火花引燃,使其完全反应,Na2O2增重7.5g,则原混合气体中O2的质量分数是
| A.54.5% | B.40% | C.36% | D.33.3% |