有A、B、C、D四种金属。将A与B用导线连接起来浸入电解质溶液中,B不易腐蚀。将A、D分别投入等浓度盐酸溶液中,D比A反应剧烈。将铜浸入B的盐溶液中,无明显变化。如果把铜浸入C的盐溶液中,有金属C析出。据此判断它们的活动性由强到弱的顺序
A. DCAB B. DABC C. DBAC D. BADC
短周期主族元素A、B、C、D原子序数依次递增,A、B、D三种元素既不同周期也不同主族,且原子的最外层电子数之和为13,B与C同周期,C的最外层电子数比B的最外层电子数多1。下列有关说法正确的是( )
A.元素D的单质只能做氧化剂
B.元素B和D可以形成化学式为BD3的共价化合物
C.A、B两种元素形成的化合物的空间构型一定是三角锥形
D.元素A、C不可能形成结构式为A—C—C—A的化合物
下列现象或反应的原理解释正确的是( )
| 选项 |
现象或反应 |
原理解释 |
| A |
铝箔在酒精灯火焰上加热熔化但不滴落 |
铝箔对熔化的铝有较强的吸附作用 |
| B |
合成氨反应需在高温条件下进行 |
该反应为吸热反应 |
| C |
镀层破损后,镀锡铁比镀锌铁易腐蚀 |
锡比锌活泼 |
| D |
2CO=2C+O2在任何条件下均不能自发进行 |
该反应ΔH>0,ΔS<0 |
下列关于常见有机物的说法中正确的是( )
| A.乙烯和苯都能使溴水褪色,褪色的原理相同 |
| B.甲烷与氯气在光照条件下反应可以制取较纯净的一氯甲烷 |
| C.乙烯和乙烷可以用酸性高锰酸钾溶液来鉴别 |
| D.苯分子中含有碳碳双键,所以苯可以和H2发生加成 |
下列离子或分子组中能大量共存,且满足相应要求的是( )
| 选项 |
离子或分子 |
要求 |
| A |
K+、OH-、淀粉、I- |
滴加氯水立即变蓝 |
| B |
Fe2+、NO3-、SO42-、H+ |
通C12后加KSCN溶液呈血红色 |
| C |
Na+、HCO3-、Ca2+、Cl- |
滴加NaOH溶液立即有沉淀产生 |
| D |
K+、NO3-、Cl-、HS- |
c(K+)<c(HS-) |
化学中常用图像直观地描述化学反应的进程或结果。下列图像描述错误的是( )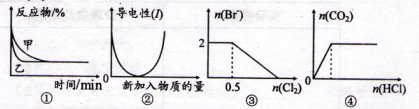
A.图①表示催化剂对可逆反应2X(g)+2Y(g) 3Z(g)+W(s)的影响,乙使用催化剂 3Z(g)+W(s)的影响,乙使用催化剂 |
| B.图②表示乙酸溶液中通人氨气至过量的过程中溶液导电性的变化 |
| C.图③表示在1 L 1 mol·L-1FeBr2溶液中通人C12时Br-的量的变化 |
| D.图④表示一定浓度NaHCO3溶液中滴加盐酸,生成CO2与滴加盐酸物质的量的关系 |