下列指定溶液中,各组离子可能大量共存的是
| A.PH=1的溶液中:K+、Fe2+、Cl-、NO3- | B.在强酸性溶液中:Cu2+、ClO-、Cl-、Ba2+ |
| C.在含有大量Fe3+的溶液中:NH4+、Cl-、Na+、AlO2- | |
D.由水电离的c(H+)=10-13mol·L-1的溶液中:Al3+、K+、NO3-、SO |
镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:
Cd + 2NiOOH + 2H2O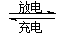 Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是
Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是
A.放电时正极反应:NiOOH + H2O- e— ="=" Ni(OH)2 + OH-
B.充电过程是化学能转化为电能的过程
C放电时Cd是负极,发生氧化反应
D.放电时电解质溶液中的OH-向正极移动
下列图像分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法中正确的是(ΔH用于表示反应中的热量变化,ΔH>0表示反应吸热 ,ΔH<0 表示反应放热)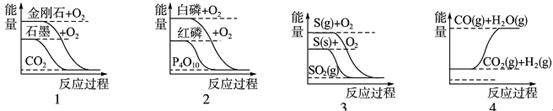
| A.石墨转变为金刚石是吸热反应 |
| B.白磷比红磷稳定 |
| C.S(g)+O2(g)===SO2(g) ΔH1S(s)+O2(g)===SO2(g) ΔH2则ΔH1>ΔH2 |
| D.CO(g)+H2O(g)===CO2(g)+H2(g) ΔH1>0 |
将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如下图所示)。在每次实验时,记录电压表指针的移动方向和电压表的读数如下表:(已知构成两电极的金属其金属活动性相差越大,电压表的读数越大)依据记录数据判断,下列结论中正确的是
| 金属 |
电子流动方向 |
电压/V |
| 甲 |
甲→Cu |
0.78 |
| 乙 |
Cu→乙 |
0.15 |
| 丙 |
丙→Cu |
1.35 |
| 丁 |
丁→Cu |
0.30 |
A.金属乙能从硫酸铜溶液中置换出铜
B.甲、乙形成合金时,将该合金露置在空气中,甲先被腐蚀
C.在四种金属中,乙的还原性最强
D.甲、丁若形成原电池时,甲为正极
在一定条件下,使10molSO3在体积固定为2L的密闭容器中发生反应:2SO2(g)+O2(g) 2SO3(g),则下图中正确的是(M表示混合气体的平均相对分子质量)
2SO3(g),则下图中正确的是(M表示混合气体的平均相对分子质量)
将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应2A(g)+B(g) 2C(g),若2 s(秒)后测得C的浓度为0.6 mol/L,现有下列几种说法:
2C(g),若2 s(秒)后测得C的浓度为0.6 mol/L,现有下列几种说法:
①用物质A表示反应的平均速率为0.3 mol/(L·s)②用物质B表示反应的平均速率为0.6 mol/(L·s)③2 s时物质A的转化率为70%④2 s时物质B的浓度为0.7 mol/L
其中正确的是
| A.①③ | B.②③ |
| C.①④ | D.③④ |