相同温度下,容积相同的甲、乙、丙3个恒容密闭容器中发生可逆反应:
2SO2(g)+O2(g) 2SO3(g);
2SO3(g);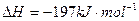 。实验测得起始、平衡时的有关数据如下表:
。实验测得起始、平衡时的有关数据如下表:
| 容器 |
起始各物质的物质的量/mol |
达到平衡时体系能量的变化 |
|||
| SO2 |
O2 |
SO3 |
Ar |
||
| 甲 |
2 |
1 |
0 |
0 |
放出热量:Q1 |
| 乙 |
1.8 |
0.9 |
0.2 |
0 |
放出热量:Q2 |
| 丙 |
1.8 |
0.9 |
0.2 |
0.1 |
放出热量 :Q3 :Q3 |
下列叙述正确的是 (  )
)
| A.Q1=Q2=Q3="197" kJ |
| B.达到平衡时,丙容器中SO2的体积分数最大 |
| C.甲、乙、丙3个容器中反应的平衡常数相等 |
| D.若在上述条件下反应生成2molSO3(s)的反应热为△H1,则△H1<-197 kJ·mol-1 |
下列溶液中的Cl—浓度与50mL1 mol/L的AlCl3溶液中的Cl—浓度相等的是()
| A.150ml 1mol/L的NaCl溶液 | B.50ml 3mol/L的 NaCl溶液 |
| C.150ml 3mol/L 的MgCl2溶液 | D.75ml 2mol/L的KCl溶液 |
2g NaOH固体溶于水配成250mL溶液,取出其中的50mL,该50mLNaOH溶液的物质的量浓度为()
| A.0.04 mol/L | B.0.2 mol/L | C.1 mol/L | D.2 mol/L |
由硫酸钾、硫酸铝和硫酸组成的混合溶液,c(H+)=0.1mol/L,c(Al3+)="0.4" mol/L, c(SO42—)="0.8" mol/L,则 c(K+)为()
| A.0.15 mol/L | B.0.2 mol/L | C.0.3 mol/L | D.0.4mol/L |
Na2CO3俗名纯碱,下面是对纯碱采用不同的分类法的分类,不正确的是()
| A.Na2CO3是盐 | B.Na2CO3是碱 |
| C.Na2CO3是钠盐 | D.Na2CO3是碳酸盐 |
一定由三种元素组成的是()
| A.氧化物 | B.碱 | C.酸 | D.盐 |