镁铝合金质优体轻,又不易锈蚀,在大量用于航空工业、造船工业、日用化工等领域。下列关于镁铝合金的性质的叙述中,正确的是
| A.此合金的熔点比镁和铝的熔点都高 |
| B.此合金能全部溶解于稀盐酸中 |
| C.此合金能全部溶解于氢氧化钠溶液中 |
| D.此合金的硬度比镁和铝的硬度都大 |
用式量为41的链状烃基取代甲苯苯环上的一个氢原子,所得芳香烃产物的数目为()
| A.3 | B.5 | C.6 | D.9 |
某有机物的结构简式如图,它在一定条件下能发生下列哪些反应()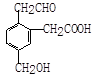
①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥消去
| A.②③④ | B.①③⑤⑥ | C.①③④⑤ | D.②③④⑤⑥ |
对下列说法不正确的是()
| A.光化学烟雾的主要成分为氮的氧化物和碳氢化合物 |
| B.工业上可以从石油裂解气中获得乙烯 |
C.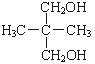 和 和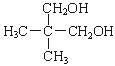 互为同分异构体 互为同分异构体 |
D.按系统命名法, 的名称为2,6-二甲基-3-乙基庚烷 的名称为2,6-二甲基-3-乙基庚烷 |
下列物质不能使溴水退色而能使酸性高锰酸钾退色的是
| A.C2H5OH | B.苯酚 | C.甲苯 | D.乙醛 |
CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都同属于离子型碳化物,请通过CaC2制C2H2的反应进行思考,从中得到必要的启示,判断下列反应产物正确的是
| A.ZnC2水解生成乙烷 | B.Al4C3水解生成甲烷 |
| C.Mg2C3水解生成丙烯 | D.Li2C2水解生成乙炔 |