I.常温下浓度均为0.l mol/L的下列溶液:①Na2CO3溶液②NaHCO3溶液③盐酸④氨水
回答下列问题。
(1)上述溶液中有水解反应发生的是 (填编号,下同),溶液中溶质存在电离平衡的是 。
(2)四种溶液中对水的电离抑制作用最大的是 ;比较①、②溶液,pH较大的是 。
(3)在溶液④中加入NH4Cl固体,NH+4浓度与OH-浓度的比值将____(填“变大”、“变小”、“不变”)
II.有一瓶无色澄清溶渡,其中可能含有:NH+4、K+、Mg2+、Al3+、Fe2+、NO-3、Cl-、SO2-4、CO2-3取该溶液进行下列实验:
(1)取部分溶液,向其中逐滴滇入Ba(OH
 )2溶液至过量,有白色沉淀生成,沉淀量与加入Ba(OH)2溶液量的关系如右图所示。
)2溶液至过量,有白色沉淀生成,沉淀量与加入Ba(OH)2溶液量的关系如右图所示。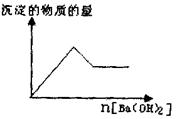
(2)取(I)反应后过滤所得沉淀和滤液,在沉淀中加入稀盐酸后,沉淀不减少。将滤液分为两等份,一份加热,未产生刺激性气味的气体;另一份如HNO3酸化时有白色沉淀产生,继续加HNO3,沉淀又消失,再加AgNO3没有变化。
根据以上事实确定:该溶液中肯定 存在的离子有 ;
存在的离子有 ;
肯定不存在的离子有____ 。
(1)标准状况下, CO2 的密度为(保留两位小数)。
的密度为(保留两位小数)。
(2)标准状况 下,由等物质的量的A 和B 两种气体组成的混合气体5.6L,其质量为7.5g。已知A的相对分子质量是B 的2.75 倍,则A 的摩尔质量为。
下,由等物质的量的A 和B 两种气体组成的混合气体5.6L,其质量为7.5g。已知A的相对分子质量是B 的2.75 倍,则A 的摩尔质量为。
(3)12.4gNa2X中含Na+ 0.4 mol,则X的相对原子质量为 。
(4)在标准状况下,一个装满氯气的容器 的质量为74.6克,若装满氮气则重66克,那么此容器的容积为。
的质量为74.6克,若装满氮气则重66克,那么此容器的容积为。
(5)在一定温度和压强下,7g氯气的体积为7.5L,在同样条件下,15L某未知气体的质量8.4 g,该未知气体的相对分子质量为。
现有m g某气体,它由双原子分子构成,它的摩尔质量为M g · mol-1。若阿伏加德罗常数用NA表示,则:
· mol-1。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________;
(2)该气体所含原子总数为____________个;
(3)该气体在标准状况下的体积为_____________;
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为_________。
2009年9月27日,热带风暴“凯萨娜”和“芭玛”造成菲律宾多个省份发生大面积洪灾和山体滑坡,超过500人死亡。洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)用化学反应方程式表示工业上制取漂白粉的原理 ;
;
(2)漂白粉的成分是(填化学式);
(3)漂白粉溶于水后,受空气中的CO2作用,即有漂白、杀菌作用,化学反应方程式为。
在一容积为2 L的密闭容器内加入0.2 mol 的N2和0.6 mol 的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图:
2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图: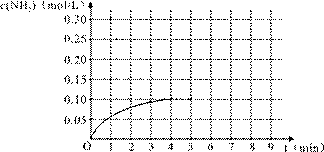
(1)根据右图,计算从反应开始到平衡时,平均反应速率v(NH3)为_____。
(2)该反应的化学平衡常数表达式K=_____。
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为________。
a. 0.20 mol/L b. 0.12 mol/L c. 0.10 mol/L d. 0.08 mol/L
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡_________________________移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数________________(填“增大”、“减小”或“不变”)。
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L)。请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。请认真观察右图,然后回答问题。
(1)图中所示反应是_________(填“吸热”或“放热”)反应,该反应_____________(填“需要”或“不需要”)加热,该反应的△H =______________________(用含E1、E2的代数式表示)。
(2)已知热化学方程式:H2(g)+ O2(g) = 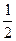 H2O(g)△H =-241.8 kJ·mol-1,该反应的活化能为167.2 kJ·
H2O(g)△H =-241.8 kJ·mol-1,该反应的活化能为167.2 kJ· mol-1,则其逆反应的活化能为____________________。
mol-1,则其逆反应的活化能为____________________。