设NA 代表阿伏加德罗常数(NA )的数值,下列说法正确的是 ( )
| A.常温常压下,1L1mol/L的亚硫酸钠溶液中的SO32-的个数为NA |
| B.标准状况下,22.4L Cl2和HCl的混合气体中含分子总数为2×6.02×1023 |
| C.标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
| D.标准状况下,22.4LSO3含分子数为NA |
现有一瓶签上注明为葡萄糖酸盐(钠、镁、钙、铁)的复合制剂,某同学为了确认其成分,取部分制剂作为试液,设计并完成了如下实验: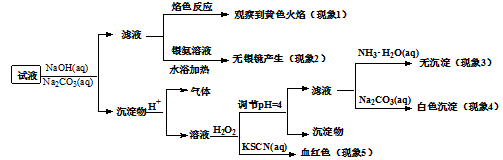
已知:控制溶液pH=4时,Fe(OH)3沉淀完全,Ca2+、Mg2+不沉淀。
该同学得出的结论正确的是
| A.根据现象1可推出该试液中含有Na+ |
| B.根据现象2可推出该试液中并不含有葡萄糖酸根 |
| C.根据现象3和4可推出该试液中含有Ca2+,但没有Mg2+ |
| D.根据现象5可推出该试液中一定含有Fe2+ |
下列分子或离子在指定的分散系中能大量共存的一组是
| A.银氨溶液: Na+、K+、NO3-、NH3·H2O |
| B.空气: C2H2、CO2、SO2、NO |
| C.氢氧化铁胶体: H+、K+、S2-、Br- |
| D.高锰酸钾溶液: H+、Na+、SO42-、葡萄糖分子 |
在水溶液中能量共存的一组离子是()
| A.Na+、Ba2+、Cl-、NO3- | B.Pb2+、Hg2+、S2-、SO42- |
| C.NH4+、H+、S2O32-、PO43- | D.ClO-、Al3+、Br-、CO32- |
在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正确的是()
| A.含等物质的量的AlO2-、OH-、CO32-的溶液中,逐滴加入盐酸:AlO2-、OH-、CO32- |
| B.含等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I-、Br-、Fe2+ |
| C.含等物质的量的Ba(OH)2、KOH的溶液中,缓慢通入CO2:KOH、Ba(OH)2、K2CO3、BaCO3 |
| D.含等物质的量的Fe3+、Cu2+、H+的溶液中加入锌粉:Fe3+、Cu2+、H+、Fe2+ |
在水溶液中能大量共存的一组离子是( )
| A.Al3+、Na+、HCO3-、SO42- | B.H+、Fe2+、ClO-、Cl- |
| C.Na+、Ag+、Cl-、SO42- | D.K+、Ba2+、NO3-、Cl- |