下列有关结构和性质的说法中,正确的是 ( )
| A.酸性:HCl>H2S,所以,非金属性:Cl>S |
B.元素原子的最外层电子数越多,越容易得电子,非金属性越 强 强 |
| C.同周期主族元素的原子形成的简单离子电子层结构一定相同 |
| D.原子核外各层电子数相等的元素一定是金属元素 |
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是
| A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| B.沉淀溶解后,将生成深蓝色的配合离子[Cu(H2O)4]2+ |
| C.该实验能证明[Cu(NH3)4]2+比氢氧化铜稳定 |
| D.在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
下列现象与氢键有关的是
①HF的熔、沸点比ⅦA族其他元素氢化物的高
②乙醇可以和水以任意比互溶
③冰的密度比液态水的密度小
④水分子高温下也很稳定
⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
| A.②③④⑤ | B.①②③⑤ | C.①②③④ | D.①②③④⑤ |
已知大多数含氧酸可用通式XOm(OH)n来表示,如X是S,则m =2,n =2,则这个式子就表示H2SO4。一般而言,该式中m大于等于2的是强酸,m为0的是弱酸。下列各含氧酸中酸性最强的是
| A.H2SeO3 | B.HMnO4 | C.H3BO3 | D.H3PO4 |
关于结构如图所示的有机物的叙述中正确的是
| A.1mol此有机物与足量Na发生反应,有3molH2生成 |
| B.分子中有3个手性碳原子 |
| C.分子中sp2、sp3杂化的原子个数比为1∶1 |
D.1mol此有机物与足量H2发生加成反应,有2mol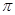 键断裂 键断裂 |
下列说法正确的是
| A.有些物质是由分子直接构成的,化学式能准确表示该物质分子组成,如白磷(P4)、二氧化碳(CO2)、氯化铵(NH4Cl)等 |
| B.C2H2与BeCl2分子中的中心原子杂化轨道的类型相同 |
| C.在1molSiO2晶体中,含有2molSi-O键 |
| D.二甲苯的沸点顺序是:邻二甲苯>对二甲苯;则羟基苯甲醛的沸点顺序是:邻羟基苯甲醛>对羟基苯甲醛 |